下列物质中,属于混合物的是( )
|
| A. | 硫酸 | B. | 蔗糖 | C. | 陈醋 | D. | 小苏打 |
分类是学习和研究化学的一种重要方法,下列分类合理的是( )
|
| A. | K2CO3和K2O都属于盐 |
|
| B. | Na2O和Na2SiO3都属于氧化物 |
|
| C. | KOH和Na2CO3都属于碱 |
|
| D. | H2SO4和HNO3都属于酸 |
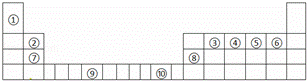
X、Y、Z、Q、M为常见的短周期元素,其原子序数依次增大.有关信息如表:
| X | 动植物生长不可缺少的元素,是蛋白质的重要成分 |
| Y | 地壳中含量居第一位 |
| Z | 短周期中其原子半径最大 |
| Q | 生活中大量使用其合金制品,工业上可用电解其氧化物的方法制备 |
| M | 海水中大量富集的元素之一,其最高正化合价与负价的代数和为6 |
(1)X的气态氢化物的大量生产曾经解决了地球上因粮食不足而导致的饥饿和死亡问题,请写出该气态氢化物的电子式 .
(2)已知37Rb和53I都位于第五周期,分别与Z和M同一主族.下列有关说法正确的是 (填序号).
A.原子半径:Rb>I B.RbM中含有共价键
C.气态氢化物热稳定性:M>I
D.Rb、Q、M的最高价氧化物对应的水化物可以两两发生反应
(3)若XM3最初水解产物是XH3和HMO,则X、M元素的电负性大小顺序是:X M((填>、<、或=);若已知磷与M元素电负性关系是:P<M,则PM3水解的化学反应方程式是 .
(4)已知QM3的熔点为190℃(2.02×105Pa),但它在180℃即开始升华,则QM3是 (填“离子化合物”或“共价化合物”),如何通过实验判 .在500K和1.01×105Pa时,它的蒸气密度(换算成标准状况时)为11.92g/L,则QM3的结构式为 .
(5)X、Y组成的一种无色气体遇空气变为红棕色.将标准状况下40L该无色气体与15L氧气通入一定浓度的NaOH溶液中,恰好被完全吸收,同时生成两种盐.请写出该反应的离子方程式 .
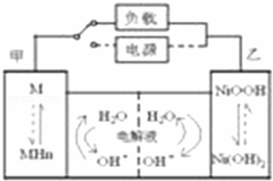
发展混合动力车是实施节能减排的重要措施之一.混合动力车的电动机目前一般使用的是镍氢电池.汽车上坡或加速时,电动机提供推动力,降低了汽油的消耗;在刹车和下坡时电动机处于充电状态以节省能耗.镍氢电池采用镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解液.镍氢电池充放电原理如图,其总反应式为:H2+2NiOOH 2Ni(OH)2下列有关混合动力车的判断正确的是( )
2Ni(OH)2下列有关混合动力车的判断正确的是( )
|
| A. | 在上坡或加速时,每消耗22.4LH2,从电极甲流向电极乙的电子是2mol |
|
| B. | 在上坡或加速时,乙电极周围溶液的pH将减小 |
|
| C. | 在刹车和下坡时,溶液中的K+向乙电极迁移 |
|
| D. | 在刹车和下坡时,甲电极的电极反应式为2H2O+2e﹣═H2↑+2OH﹣ |
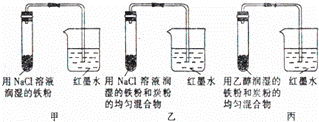
若图1是在金属锌板上贴上一张用某溶液浸湿的滤纸,图2是NaBH4/H2O2燃料电池,则下列的说法中正确的是( )
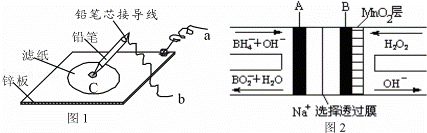
|
| A. | 图2电池在放电过程中,正极区的电极反应为:BH4﹣﹣8e﹣+8OH﹣═BO2﹣+6H2O |
|
| B. | 若用稀硫酸浸湿滤纸并用导线将a、b相连,则有电子从b极流出通过导线流向a极 |
|
| C. | 若用硫酸钠和紫色石蕊的混合溶液浸湿滤纸并用导线将a、b相连,则可看到铅笔芯C点处浸有紫色石蕊的滤纸变蓝,此处发生电极反应为:O2+2H2O+4e﹣═4OH﹣ |
|
| D. | 若用KI﹣淀粉溶液浸湿滤纸,同时用导线将a、b分别与A、B电极相连,若看到铅笔芯C点处出现变蓝现象,则b极连接的是燃料电池的A极 |
某同学按如图所示的装置进行电解实验.下列说法不正确的是( )
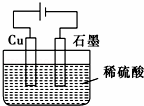
|
| A. | 电解过程中,铜电极上有H2产生 |
|
| B. | 电解初期,总反应方程式为Cu+H2SO4 |
|
| C. | 电解一定时间后,石墨电极上有铜析出 |
|
| D. | 整个电解过程中,溶液pH值会增大 |
控制适合的条件,将反应2Fe3++2I﹣⇌2Fe2++I2设计成如图所示的原电池.下列判断不正确的是( )
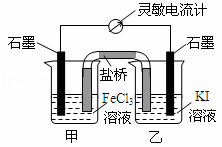
|
| A. | 反应开始时,乙中石墨电极上发生氧化反应 |
|
| B. | 反应开始时,甲中石墨电极上Fe3+被还原 |
|
| C. | 电流计读数为零时,反应达到化学平衡状态 |
|
| D. | 电流计读数为零后,在甲中溶入FeCl2固体,乙中石墨电极为负极 |
 CuSO4+H2↑
CuSO4+H2↑