草酸晶体的组成可表示为H2C2O4•xH2O.实验室常用其加热分解制取CO气体,反应方程式为:H2C2O4•xH2O  CO+CO2+(x+1)H2O.下图为分解草酸晶体,用干燥纯净的CO还原CuO制取Cu,并收集CO的实验装置(略去铁架台、铁夹等支撑加持装置),回答下列问题.
CO+CO2+(x+1)H2O.下图为分解草酸晶体,用干燥纯净的CO还原CuO制取Cu,并收集CO的实验装置(略去铁架台、铁夹等支撑加持装置),回答下列问题.
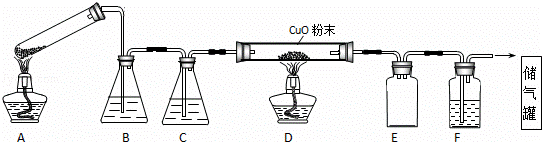
(1)A装置为加热分解草酸的装置,该装置错误是 试管口应向上倾斜(或应向下倾斜) ,C装置中盛放的试剂是 浓硫酸 (填化学式),E装置的作用是 安全瓶(或防倒吸) .
(2)实验过程中涉及到如下操作:①点燃A处的酒精灯 ②熄灭A处的酒精灯 ③点燃D处的酒精灯 ④熄灭D处的酒精灯.这4步操作由先到后的顺序为 ①③④② (填序号).点燃D处酒精灯前必须要进行的操作名称是 验纯 .
(3)用酸性高锰酸钾溶液滴定草酸晶体,求x的值.
实验步骤:准确称取1.17g 草酸晶体,配成100mL溶液;取出20.00mL于锥形瓶中,再向瓶中加入足量稀H2SO4;用0.0500mol/L酸性高锰酸钾溶液滴定,滴定至终点时消耗高锰酸钾溶液16.00mL.滴定时,所发生的反应为:2MnO4﹣+5H2C2O4+6H+=10CO2+2Mn2++8H2O.
①配制草酸溶液除需要玻璃棒、烧杯,还一定需要的玻璃仪器有 100mL容量瓶、胶头滴管 .
②x= 1.5 .
(4)为探究催化剂对化学反应速率的影响,在甲乙试管中分别加入下列物质
| 试管 | 0.01mol/L KMnO4 | 0.1mol/L H2C2O4 | 0.1mol/L H2SO4 | MnSO4固体 |
| 甲 | 4mL | x mL | 1mL | 无 |
| 乙 | y mL | 2mL | 1mL | 有 |
则x= 2 ,y= 4 .能够得出催化剂对该反应有影响结论的实验现象是 加入MnSO4固体的试管中溶液褪色速率比未加的快 .
室温下,用0.1mol/L氨水分别滴定20.0mL、0.1mol/L的盐酸和醋酸,曲线如图所示,下列说法正确的( )

|
| A. | I曲线表示的是滴定盐酸的曲线 |
|
| B. | x=20 |
|
| C. | 滴定过程中 |
|
| D. | 当I曲线和II曲线pH均为7时,一溶液中的c(Cl﹣)等于另一溶液中的c(CH3COO﹣) |
下列实验方案、现象和结论均正确的是( )
| 选项 | 实验方案 | 现象 | 结论 |
| A |
| 向里推活塞时,长颈漏斗中有一段水柱,静止,水柱高度不变 | 该装置的气密性良好 |
| B |
| 脱脂棉燃烧 | Na2O2与水反应生成氢氧化钠和氧气 |
| C |
| 烧杯①的澄清石灰水先变浑浊 | NaHCO3比Na2CO3受热更易分解 |
| D |
| U形管右端的液面高 | 铁钉发生吸氧腐蚀 |
|
| A. | A | B. | B | C. | C | D. | D |
等质量的氯气与下列足量物质反应,转移的电子数最少的是( )
|
| A. | 冷的NaOH溶液 | B. | SO2的水溶液 | C. | FeCl2溶液 | D. | 铜 |
下列关于离子的叙述正确的是( )
|
| A. | 在c(H+)=1×10﹣13mol•L﹣1的溶液中:Na+、Fe3+、Cl﹣、SO42﹣能大量共存 |
|
| B. | 铜溶于FeCl3溶液中:Cu+Fe3+=Fe2++Cu2+ |
|
| C. | NaHCO3溶液中:c(Na+)=c(CO32﹣)+c(HCO3﹣)+c(H2CO3) |
|
| D. | 向溶液中加入BaCl2溶液后再加盐酸,有白色沉淀,说明该溶液中一定含有SO42﹣ |


 的相对分子质量大2,则符合下列条件的G的同分异构体有 3 种.
的相对分子质量大2,则符合下列条件的G的同分异构体有 3 种.
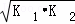 (用K1、K2表示)
(用K1、K2表示)
 的值逐渐减小
的值逐渐减小


