碳素利用是环保科学家研究的热点课题。
I.某研究小组现将三组CO(g)与H2O(g)的混合气体分别通入体积为2L的恒容密闭容器中,一定条件下发生反应:CO(g)+H2O(g) CO2(g)+H2(g) △H<0,得到如下数据:
CO2(g)+H2(g) △H<0,得到如下数据:
| 实验组 | 温度/℃ | 起始量(mol) | 平衡量(mol) | 达到平衡所 需要时间/min | ||
| CO(g) | H2O(g) | CO2(g) | H2(g) | |||
| I | 800 | 2 | 2 | x | 1 | 5 |
| II | 900 | 1 | 2 | 0.5 | 0.5 | T1 |
| III | 900 | 2 | 2 | a | a | T2 |
(1)实验I中,前5min的反应速率υ(CO2)= 。
(2)下列能判断在800℃实验条件下CO(g)与H2O(g)反应一定达到平衡状态的是 。
A.容器内压强不再变化 B.n2(H2)= n(H2O)·n(CO)
C.混合气体密度不变 D.υ正(CO) =υ逆(CO2)
(3)实验II和III中CO的平衡转化率:αII(CO) αIII(CO) (填:>、<或=,下同) ,T1 T2,a= (填精确数值)。
 (4)若实验Ⅲ的容器改为在绝热的密闭容器中进行,实验测得H2O(g)的转化率随时间变化的示意图如下图所示, b点υ正 υ逆(填“<”、“=”或“>”),t3~t4时刻,H2O(g)的转化率H2O%降低的原因是 。
(4)若实验Ⅲ的容器改为在绝热的密闭容器中进行,实验测得H2O(g)的转化率随时间变化的示意图如下图所示, b点υ正 υ逆(填“<”、“=”或“>”),t3~t4时刻,H2O(g)的转化率H2O%降低的原因是 。
(5)CO和H2在一定条件下合成甲醇。
甲醇/空气碱性燃料电池中,
消耗32g甲醇,电池中有转移4.5 mol电子。
负极的电极反应式为 。
该电池中电流效率为 。
(电流效率η= ×100%)
×100%)
二氧化锰在生产、生活中有广泛应用。
(1)锌—锰碱性电池广泛应用于日常生活。电池的总反应式为
Zn(s)+2MnO2(s)+2H2O(l)===Zn(OH)2(s)+2MnOOH(s)。
该电池的正极反应式为 。
(2)某学习小组拟以废旧干电池为原料制取锰,简易流程如下:
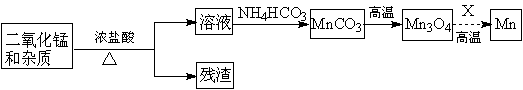
①加入浓盐酸溶于废旧电池内黑色物质过程中保持通风,其原因是 。
②从产品纯度、环保等角度考虑,X宜选择 (填代号)。
A.焦炭 B.铝 C.氢气 D.一氧化碳
③写出碳酸锰在空气中灼烧生成四氧化三锰的化学方程式 。
(3)电解硫酸锰溶液法制锰又叫湿法冶锰。以菱锰矿(主要成份是MnCO3,主要杂质是Fe2+、Co2+、Ni2+)为原料制备锰的工艺流程如下:
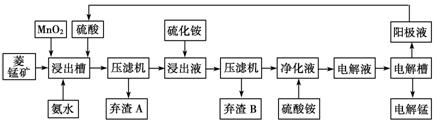
已知:NiS 、CoS均难溶于水。部分氢氧化物的pH如下表:(若某离子浓度小于等于105mol·L1,则认为完全沉淀)
| 物质 | Fe(OH)2 | Ni(OH)2 | Co(OH)2 | Mn(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 7.5 | 7.7 | 7.6 | 8.3 | 2.7 |
| 完全沉淀pH | 9.7 | 8.4 | 8.2 | 9.8 | 3.8 |
①用离子方程式表示加入二氧化锰的作用 。
②加入氨水调节浸出槽中溶液的pH范围: 。
③弃渣B可能含有的物质为 。
④电解槽阴极的电极反应式为 。
下表中的陈述均正确并且前后存在因果关系的是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | SO2有漂白性 | SO2可使溴水和酸性高锰酸钾溶液褪色 |
| B | Fe3+有强氧化性 | FeCl3溶液可用于回收废旧电路板中的铜 |
| C | 浓硫酸有吸水性 | 浓硫酸可使蔗糖和纸张碳化变黑 |
| D | SiO2有导电性 | SiO2可用于制备光导纤维 |
根据下列反应所画图象错误的是( )
| A | B | C | D |
| 将二氧化硫通入 到一定量氯水中 | 将氨水滴入到一定 量氯化铝溶液中 | 将铜粉加入到 一定量浓硝酸中 | 将铁粉加入到一 定量氯化铁溶液中 |
|
|
|
|
|
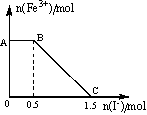
向甲溶液中缓慢滴加乙溶液,反应生成沉淀的质量如下图所示,其中符合图像的一组是( )
| 甲 | 乙 |
| |
| A | AlCl3、Mg(NO3)2、HNO3 | NaOH | |
| B | Na2CO3、NH4HCO3、Na2SO4 | Ba(OH)2 | |
| C | NH4NO3、Al(NO3)3、Fe(NO3)3、HCl | NaOH | |
| D | NaAlO2、氨水、NaOH | H2SO4 |
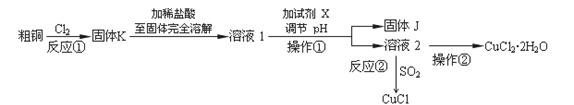
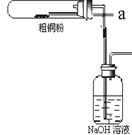 (夹持仪器和加热装置省略)。观察到的现象是 ,
(夹持仪器和加热装置省略)。观察到的现象是 ,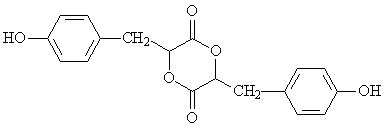
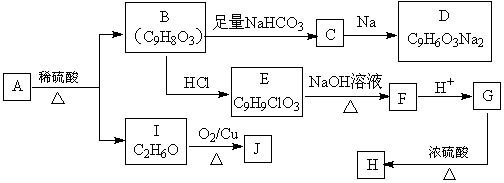
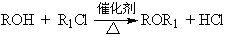
 ①C 、CO ② S、SO2
①C 、CO ② S、SO2