含氮化合物对人类生活有十分重大的意义。
(1)目前广泛使用的工业合成氨方法是用氮气和氢气在一定条件下化合。
已知:N2(g)+O2(g) =2NO(g) △H=+180.5kJ/mol
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=-905kJ/mol
2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ/mol
①写出工业合成氨的热化学方程式: 。
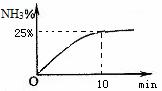 ②实验室模拟合成氨,在2L密闭容器中投入1molN2 和3mol H2,容器中氨气的体积分数随时间变化如图所示。则0~10min,NH3的平均速率为 ;达平衡时,N2的转化率为 。
②实验室模拟合成氨,在2L密闭容器中投入1molN2 和3mol H2,容器中氨气的体积分数随时间变化如图所示。则0~10min,NH3的平均速率为 ;达平衡时,N2的转化率为 。
③若在②达平衡后,保持容器体积及温度不变,移走0.5molNH3,再达平衡时,N2的体积分数将 ,平衡常数 (填“增大”“减小”或“不变”)
(2)科学家一直致力于研究常温常压下“人工固氮”的方法。据报道:在常温常压条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水反应,生成NH3和一种单质。进一步研究NH3生成量与温度关系,部分实验数据如下(反应时间3h,其余条件一样)
| T/℃ | 30 | 40 | 50 |
| NH3生成量/10-6mol | 4.8 | 5.9 | 6.0 |
①写出常温下“人工固氮”反应的化学方程式: _
此反应△H 0(填“>”、“<”或“=)。
②该反应中的催化剂TiO2的制取方法之一是将TiCl4气体导入氢氧火焰中(700~1000℃)进行水解。写出TiCl4水解的化学方程式: 。
③在上述固氮过程中,除加入催化剂外,能提高生产速率,但不降低产率的措施还可以是 。
A.适当升高温度 B.将氨气液化分离
C.增大反应物N2的浓度 D.增大压强
查文献知,CH3COOH、H3PO3(二元酸)、H3PO4三种酸所有的逐级电离常数如下:
| 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) |
| CH3COOH | 1.8×10-5 | H3PO4 | K1=7.1×10-3 |
| H3PO3 | K1=3.7×10-2 | K2=6.2×10-8 | |
| K2 =2.9×10-7 | K3=4.5×10-13 |
用化学用语回答下列问题:
(1)上述三种酸中,酸性最强的是 ;
(2)常温下,在NaH2PO3稀溶液中:c(H3PO3) < c(HPO32-),则该溶液pH_______7;(填“>”“<”或“=”)
(3)等温度、等浓度的NaH2PO4溶液与Na2HPO4溶液比较,c(H3PO4)较大的是:___ __;
(4)25℃时,浓度均为0.01 mol/L 的CH3COONa、Na2HPO3、Na3PO4溶液,pH最大的是:_________________;
(5)在NaH2PO3溶液中,粒子间存在等量关系:c(H3PO3)+_____________= c(Na+)。(用溶液中其它粒子浓度补充完整)
 2NH3的反应速率可以分别用v(H2)、v(N2)、v(NH3)(单位为mol·L-1·s-1)表示,则下
2NH3的反应速率可以分别用v(H2)、v(N2)、v(NH3)(单位为mol·L-1·s-1)表示,则下 (1)图I表示10mL量筒中液面的位置,A与B、B与C刻度相差1mL,如果刻度A为5,量筒中液体体积是 mL。
(1)图I表示10mL量筒中液面的位置,A与B、B与C刻度相差1mL,如果刻度A为5,量筒中液体体积是 mL。 2C(g)(正反应吸热),下列图象中正确的是( )
2C(g)(正反应吸热),下列图象中正确的是( )
 B. 1
B. 1
 D.
D. 