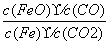一定温度下,在容积为2 L的密闭容器中发生反应CO(g)+H2O(g)  CO2(g)+H2(g),部分数据见下表(表中t2>t1)。
CO2(g)+H2(g),部分数据见下表(表中t2>t1)。
| 反应时间/min | n(CO) /mol | n(H2O) /mol | n(CO2) /mol | n(H2) /mol |
| 0 | 1.20 | 0.60 | 0 | 0 |
| t1 | 0.80 | |||
| t2 | 0.20 |
下列说法正确的是 ( )
A.反应在t1 min内的反应速率为v(H2)= mol·L-1·min-1
mol·L-1·min-1
B.平衡时CO的转化率为66.67%
C.该温度下反应的平衡常数 为1
为1
D.其他条件不变,若起始时n(CO)=0.60 mol,n(H2O)=1.20 mol,则平衡时n(CO2)=0.20 mol
在300 mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)  Ni(CO)4(g),已知该反应的平衡常数与温度的关系如下表:
Ni(CO)4(g),已知该反应的平衡常数与温度的关系如下表:
| 温度/℃ | 25 | 80 | 230 |
| 平衡常数 | 5×104 | 2 | 1.9×10-5 |
下列说法不正确的是 ( )
A.上述生成Ni(CO)4的反应为放热反应
B.25 ℃时反应Ni(CO)4(g)  Ni(s)+4CO(g)的平衡常数为2×10
Ni(s)+4CO(g)的平衡常数为2×10 -5
-5
C.在80 ℃时,测得某时刻Ni(CO)4、CO的浓度均为0.5 mol·L-1,则此时v正>v逆
D.80 ℃达到平衡时,测得n(CO)=0.3 mol,则Ni(CO)4的平衡浓度为2 mol·L-1
在0.5 L的密闭容器中,一定量的氮气与氢气进行如下反应:N2(g)+3H2(g)
2NH3(g) ΔH=a kJ·mol-1,其化学平衡常数K与温度的关系如下。
| 温度/℃ | 200 | 300 | 400 |
| K | 1.0 | 0.86 | 0.5 |
请回答下列问题。
(1)写出该反应的化学平衡常数表达式:_______________________________,a________(填“大于”、“小于”或“等于”)0。
(2)400 ℃时,2NH3(g)  N2(g)+3H2(g)的化学平衡常数为__________,测得氨气、氮气、氢气的物质的量分别为3 mol、2 mol、1 mol时,该反应的v正(N2)________(填“大于”、“小于”或“等于”)v逆(N2)。
N2(g)+3H2(g)的化学平衡常数为__________,测得氨气、氮气、氢气的物质的量分别为3 mol、2 mol、1 mol时,该反应的v正(N2)________(填“大于”、“小于”或“等于”)v逆(N2)。
 3Z(g)
3Z(g) 
 CH3OH(g) ,△H<0
CH3OH(g) ,△H<0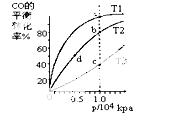 确的是( )
确的是( ) 2NH3,若将平衡体系中各物质的浓度都增加到原来的2倍,则产生的结果是
2NH3,若将平衡体系中各物质的浓度都增加到原来的2倍,则产生的结果是