某化学活动小组设计如下图所示(部分夹持装置已略去)实验装置,以探究潮湿的Cl2与Na2CO3反应得到的固体物质的成分。
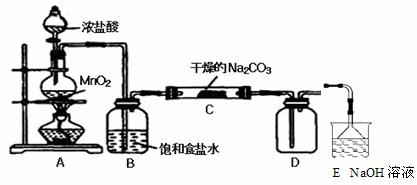
向C装置中通入一定量的氯气后,测得只生成一种气体Cl2O。可以确定的是C得到的固体最多含有三种物质,含有氯元素的盐只有一种,且一定含有NaHCO3,现对C中得到的固体成分进行猜想和验证。
①提出合理猜想:一定含有NaHCO3和 ;可能含有剩余的Na2CO3。
②设计方案,进行成分检验:
请完成实验步骤3、4以及预期现象和结论并将答案填入下表的相应空格内。
限选实验试剂:蒸馏水、稀HNO3、BaCl2溶液、澄清石灰水、AgNO3溶液、品红、稀盐酸
| 实 验 步 骤 | 预 期 现 象 和 结 论 |
| 步骤1:取C中的少量固体样品于试管中,加入蒸馏水至固体溶解,然后各取1~2mL所得溶液分别置于甲、乙两支试管中。 | 得到无色溶液 |
| 步骤2:向甲试管中加入过量的BaCl2溶液,静置。 | 若溶液变浑浊,证明固体中含有 。 |
| 步骤3:取甲试管中上层清液少许于另一只试管中,滴加少量 ,充分振荡。 | 若 , 证明固体中含有NaHCO3 。 |
| 步骤4:向乙试管中先加入过量的 , 再滴入少量 溶液。 | 若生成白色沉淀;证明固体中含有______。 |
Na、Cu、O、Si、S、Cl是常见的六种元素。
(1)Na位于元素周期表中 ;S的基态原子核外有 个未成对电子;Si的基态原子核外电子排布式为 。
(2)用“>”或“<”填空:
| 第一电离能 | 离子半径 | 熔点 | 酸性 |
| Si S | O2- Na+ | NaCl Si | H2SO4 HClO4 |
(3)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101KPa下,已知该反应每消耗1 mol CuCl(s),放热44.4KJ,该反应的热化学方程式是 。
(4)ClO2是常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式 。
X、Y、Z、W、Q、R六种短周期主族元素,原子序数依次增大,Z基态原子核外有三个未成对电子,Y、Z、W分别与X形成常见化合物的分子结构依次为正四面体、三角锥形和V形。Q的各级电离能如下表,W与R是同族元素。
| Q | I1 | I2 | I3 | I4 | I5 | … |
| 电离能(kJ/mol) | 496 | 4562 | 6912 | 9543 | 13353 | … |
回答下列有关问题:
(1)W形成单质的晶体类型是_____________;其单核离子结构示意图为_____________。
(2)化合物Q2W2的电子式__________,化合物XYZ的结构式________________。
(3)Y与X形成式量最小,且分子中含有非极性键的分子式__________。

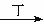 乙
乙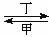 丙。下列有关物质的推断不正确的是
丙。下列有关物质的推断不正确的是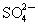 的物质的量浓度为0.7 mol/L,则此溶液中Na+的物质的量浓度为
的物质的量浓度为0.7 mol/L,则此溶液中Na+的物质的量浓度为