相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:
2SO2(g)+O2(g)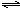 2SO3(g) △H=-196.4kJ·mol-1
2SO3(g) △H=-196.4kJ·mol-1
实验测得起始、平衡时的有关数据如下表:
| 容器编号 | 起始时各物质物质的量/mol | 平衡时反应中 的能量变化 | ||
| SO2 | O2 | SO3 | ||
| ① | 2 | 1 | 0 | 放出热量a kJ |
| ② | 1 | 0.5 | 0 | 放出热量b kJ |
| ③ | 0 | 0 | 2 | 吸收热量c kJ |
下列叙述不正确的是
A.平衡时SO3气体的体积分数:③=①>② B.a+c=196.4
C.三个容器内反应的平衡常数:③=①=② D.平衡时O2的浓度:①=③=2×②
已知常温下,浓度均为0.1 mol·L-1的4种钠盐溶液pH如下表:
| 溶质 | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
| pH | 11.6 | 9.7 | 10.3 | 5.2 |
下列说法中正确的是
A.足量SO2通入NaClO溶液中发生反应的离子方程式为:H2O+SO2+ClO-=HClO+HSO3-
B.向氯水中加入NaHCO3,可以增大氯水中次氯酸的浓度
C.常温下,相同物质的量浓度的H2SO3、H2CO3、HClO溶液,pH最大的是H2SO3
D.NaHSO3溶液中离子浓度大小顺序为:c(Na+)> c(H+)>c(HSO3-) >c(SO32-)>c(OH-)
下列有关物质的应用不正确的是
A.碳酸氢钠具有弱碱性,可治疗胃酸过多
B.氧化镁熔点高,可做耐高温材料
C.二氧化硫具有漂白性,可用于漂白纸浆和草帽辫
D.二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸
 不正确的是
不正确的是  (HCO3)2 +2NaOH(过量) = MgCO3↓+ Na2CO3+ 2H2O
(HCO3)2 +2NaOH(过量) = MgCO3↓+ Na2CO3+ 2H2O +H+(aq)= H2O(l) ΔH
+H+(aq)= H2O(l) ΔH mol·L-1的溶液中:[Ag(NH3)2]+、Na+、Fe2+、AlO2-、I-
mol·L-1的溶液中:[Ag(NH3)2]+、Na+、Fe2+、AlO2-、I-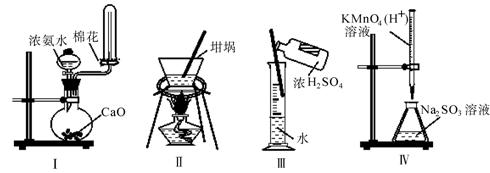
 标准溶液滴定未知浓度的Na2SO3溶液
标准溶液滴定未知浓度的Na2SO3溶液