人体血液里存在重要的酸碱平衡:CO2+H2OH2CO3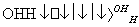 HCO
HCO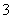 ,使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随c(HCO
,使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随c(HCO )∶c(H2CO3)变化关系如下表:
)∶c(H2CO3)变化关系如下表:
| c(HCO | 1.0 | 17.8 | 20.0 | 22.4 |
| pH | 6.10 | 7.35 | 7.40 | 7.45 |
下列说法不正确的是( )
A.正常人体血液中,HCO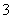 的水解程度大于电离程度
的水解程度大于电离程度
B.人体血液酸中毒时,可注射NaHCO3溶液缓解
C.pH=7.00的血液中,c(H2CO3)>c(HCO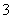 )
)
D.pH=7.40的血液中,HCO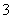 的水解程度一定大于H2CO3的电离程度
的水解程度一定大于H2CO3的电离程度
在T℃时,某NaOH稀溶液中c(H+)=10-a mol·L-1,c(OH-)=10-b mol·L-1,已知a+b=12。向该溶液中逐滴加入pH=c的盐酸(T℃),测得混合溶液的部分pH如下表所示:
| 序号 | NaOH溶液体积 | 盐酸体积 | 溶液pH |
| ① | 20.00 | 0.00 | 8 |
| ② | 20.00 | 20.00 | 6 |
假设溶液混合前后的体积变化忽略不计,则c为( )
A.1 B.4
C.5 D.6
Ⅰ.25℃时,三种酸的电离常数为:
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数K | 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
请回答下列问题:
(1)物质的量浓度为0.1 mol/L的下列物质:a.Na2CO3、b.NaClO、c.CH3COONa、d.NaHCO3;pH由大到小的顺序是:________(填编号)
(2)常温下0.1 mol/L的CH3COOH电离度约为1%,其pH=________,将该溶液加蒸馏水稀释,在稀释过程中,下列表达式的数据变大的是:________。
A.c(H+) B.c(H+)/c(CH3COOH)
C.c(H+)·c(OH-) D.c(OH-)/c(H+)
(3)体积为10 mL pH=2的醋酸溶液与一元酸HX分别加蒸馏水稀释至1 000 mL,稀释过程pH变化如图;则HX的电离平衡常数________(填“大于”、“等于”或“小于”)醋酸的电离平衡常数;稀释后,HX溶液中水电离出来的c(H+)________醋酸溶液水电离出来的c(H+)(填“大于”、“等于”或“小于”)。

(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中:c(CH 3COO-)-c(Na+)=________(填准确数值)。
3COO-)-c(Na+)=________(填准确数值)。
Ⅱ.锶(Sr)为第五周期ⅡA族元素。高纯六水氯化锶晶体(SrCl2·6H2O)具有很高的经济价值,61℃时晶体开始失去结晶水,100℃时失去全部结晶水。用工业碳酸锶粉末(含少量Ba、Fe的化合物)制备高纯六水氯化锶的过程如下图。

请回答:
(5)步骤③中调节溶液pH至8~10,宜选用的试剂为________。
A.稀硫酸 B.氢氧化锶粉末
C.氢氧化钠 D.氧化锶粉末
所得滤渣的主要成分是________(填化学式)。
(6)若滤液中Ba2+ 浓度为1×10-5mol·L-1,依据下表数据可以推算滤液中Sr2+物质的量浓度为________。
| SrSO4 | BaSO4 | Sr(OH)2 | Fe(OH)3 | Fe(OH)2 | |
| Ksp | 3.3×10-7 | 1.1 × 10-10 | 3.2 × 10-4 | 2.6× 10-39 | 4.87× 10-17 |

 )
)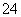 )>c(H+)>c(OH-)
)>c(H+)>c(OH-)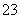 +H2O
+H2O