向一定体积的密闭容器中加入2 mol A、0.6 mol C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如图(Ⅰ)所示,其中t0~t1阶段c(B)未画出。图(Ⅱ)为t2时刻后改变反应条件,化学反应速率随时间变化的情况,四个阶段改变的条件均不相同,每个阶段只改变浓度、温度、压强、催化剂中的一个条件,其中t3~t4阶段为使用催化剂。
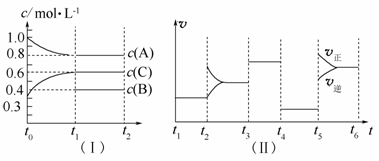
请回答下列问题:
(1)若t1=15 min,则t0~t1阶段以C物质的浓度变化表示反应速率为____________________________。
(2)t4~t5阶段改变的条件为__________,B的起始物质的量浓度为__________。各阶段平衡时对应的平衡常数如下表所示:
| t1~t2 | t2~t3 | t3~t4 | t4~t5 | t5~t6 |
| K1 | K2 | K3 | K4 | K5 |
则K1=__________(保留两位小数),K1、K2、K3、K4、K5之间的关系为________________________(用“>”、“<”或“=”连接)。
(3)t5~t6阶段保持容器内温度不变,若A的物质的量共变化了0.01 mol,而此过程中容器与外界的热交换总量为a kJ,写出此温度下该反应的热化学方程式__________________________________。
(4)在相同条件下,若起始时容器中加入a molA、b mol B和c mol C,要达到t1时刻同样的平衡,a、b、c要满足的条件为__________________________________________________________。
如图,p、q为直流电源两极,A由+2价金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D产生气泡。试回答:
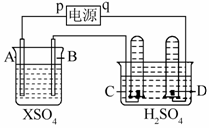
(1)p为__________极,A极发生了__________(填反应类型)反应。
(2)C为__________极,试管里收集到__________;D为__________极,试管里收集到__________。
(3)C极的电极方程式是_________________________________。
(4)在电解过程中,测得C、D两极上产生的气体实验数据如下:
| 时间(min) | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 阴极生成 气体体积(cm3) | 6 | 12 | 20 | 29 | 39 | 49 | 59 | 69 | 79 | 89 |
| 阳极生成 气体体积(cm3) | 2 | 4 | 7 | 11 | 16 | 21 | 26 | 31 | 36 | 41 |
仔细分析上表,请说出得到以上实验数据可能的原因是_________________________________________________________。
(5)当电路中通过0.004 mol电子时,B电极上沉积金属X的质量为0.128 g,则此金属的摩尔质量为______________________。
(6)当反应进行一段时间后,A、B电极附近溶液的pH__________(填“增大”“减小”或“不变”)。




