Ⅰ. 在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)  2Z(g) △H < 0,一段时间后达到平衡,反应过程中测定的数据如下表:
2Z(g) △H < 0,一段时间后达到平衡,反应过程中测定的数据如下表:
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12[来源:Z§xx§k.Com] | 0.11 | 0.10 | 0.10 |
(1)反应前2min的平均速率ν(Z)= ,该温度下此反应的平衡常数K=
(2)其他条件不变,若降低温度,反应达到新平衡前ν(逆) ν(正) (填“>”,“<”或“=”)
(3)其他条件不变,若再充入0.2molZ,平衡时X的体积分数 (填“增大”,“减小”或“不变”)
Ⅱ. 某电解池装置如下图所示:

(1)外电源的负极是 (填“X”或“Y”)
(2)阳极室中发生的反应依次为 ,
(3)若外电路转移0.02mol电子,则膜两侧溶液质量变化差△m左 – △m右= g
X、Y、Z是三种气态物质,在一定温度下其变化符合下图。下列说法不正确的是
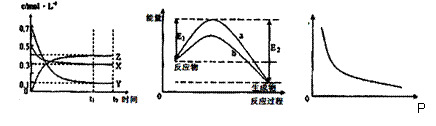 |
 图I 图II 图III
图I 图II 图III
 A.该反应的化学方程式为X(g) +3Y(g) 2Z(g)
A.该反应的化学方程式为X(g) +3Y(g) 2Z(g)
B.图III中的纵坐标可表示混合气体中Z的含量或者混合气体的平均摩尔质量
C.若升高温度,该反应的平衡常数减小,Y的转化率降低
D.图II中曲线可表示有无催化剂的能量变化曲线
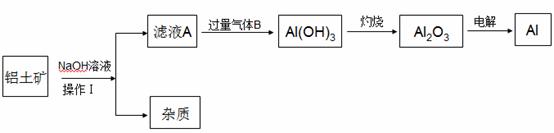
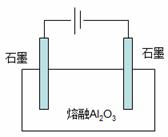 (3)工业上采用右图装置电解熔融Al2O3制备金属铝,该电
(3)工业上采用右图装置电解熔融Al2O3制备金属铝,该电 __; 与W同主族且半径比W小的元素所形成的氢化物B,A的沸点比B的沸点 (填“高”或“低”),原因是
__; 与W同主族且半径比W小的元素所形成的氢化物B,A的沸点比B的沸点 (填“高”或“低”),原因是 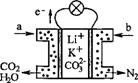 某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理见右图。下列说法正确的是
某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理见右图。下列说法正确的是