只给出下列甲和乙中对应的量,不能求出物质的量的是 ( )
| A | B | C | D | |
| 甲 | 物质的粒子数 | 标准状况下的气体摩尔体积 | 固体的体积 | 溶液中溶质的物质的量浓度 |
| 乙 | 阿伏加德罗常数 | 标准状况下的气体体积 | 固体的密度 | 溶液的体积 |
紫菜与海带类似,是一种富含生物碘的海洋植物.商品紫菜轻薄松脆、比海带更易被焙烧成灰(此时碘转化为碘化物无机盐),用于碘单质的提取.已知:
| 乙醇 | 四氯化碳 | 裂化汽油 | 碘(晶体) | |
| 密度/g•cm﹣3 | 0.7893 | 1.595 | 0.71~0.76 | 4.94 |
| 沸点/℃ | 78.5 | 76.8 | 25~232 | 184.35 |
以下为某兴趣小组模拟从紫菜提取碘单质的过程:
紫菜→(焙烧)→(浸取) (操作①)
(操作①) (操作②)→(蒸馏)→粗产品
(操作②)→(蒸馏)→粗产品
(1)实验室中焙烧紫菜用到的仪器有 CEF .
A.烧杯 B.蒸发皿 C.坩埚 D.试管 E.酒精灯 F.泥三角
(2)将焙烧所得的紫菜灰与足量的双氧水和稀硫酸作用,写出反应的离子方程式 2I﹣+H2O2+2H+═I2+2H2O .
(3)操作①的名称是 过滤 ;试剂A为 四氯化碳 (填本题表格中一种最佳化学试剂的名称),不使用另外两种试剂的主要原因分别是:
Ⅰ 乙醇与水互溶 ;
Ⅱ 裂化汽油能与碘发生加成反应 .
(4)操作②应在 分液漏斗 (仪器名称)中振荡、静置,操作时先分离出的是 下层液体 .
(5)将下列装置图中缺少的必要仪器补画出来以最终将单质碘与试剂A分离:
已知某气体反应的平衡常数可表示为K=c(CH3OCH3)c(H2O)/[c(CH3OH)]2,该反应在不同温度下的平衡常数:400℃,K=32;500℃,K=44.
请回答下列问题:
(1)写出上述反应的化学方程式 2CH3OH(g) CH3OCH3(g)+H2O(g) .
CH3OCH3(g)+H2O(g) .
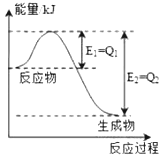
(2)该反应的正反应是 吸热 反应(填“放热”或者“吸热”),
(3)已知在密闭容器中,测得某时刻各组分的浓度如下:
| 物质 | CH3OH(g) | CH3OCH3(g) | H2O(g) |
| 浓度/(mol•L﹣1) | 0.54 | 0.68 | 0.68 |
①此时系统温度400℃,比较正、逆反应速率的大小:v正 > v逆 (填“>”、“<”或“=”).
②若以甲醇百分含量为纵坐标,以温度为横坐标,此时反应点在图象的位置是图中 A 点.比较图中B、D两点所对应的正反应速率B < D(填“>”、“<”或“=”).理由是 D点温度高于B点,温度越高反应速率越大,所以反应速率也大于B .
(4)一定条件下要提高反应物的转化率,可以采用的措施是 ae
a.升高温度 b.加入催化剂 c.压缩容器的体积
d.增加水蒸气的浓度 e.及时分离出产物.

T℃,向5L恒容密闭容器中充入1molSO3气体,发生反应2SO3(g)⇌2SO2(g)+O2(g)
△H=+196kJ/mol,一段时间后达到平衡,测得此过程中从外界共吸收了19.6kJ的热量.当温度度不变时,改变某一条件,下列结论正确的是( )
| 条件改变 | 结论 | |
| A | 平衡后向容器中冲入1molHe | 平衡常数不变,混合气体的密度也不变 |
| B | 起始时向容器中冲入0.5molSO2、0.25molO2和2molSO3 | 反应达到平衡前v(正)>v(逆) |
| C | 起始时向容器中充入1molSO2和0.5mol O2 | 达到平衡时共放出78.4kJ的热量 |
| D | 起始时向容器中充入1molSO2和0.5molO2 | 达到平衡时,SO2的转化率为60% |
|
| A. | A | B. | B | C. | C | D. | D |

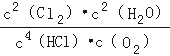 ;若反应容器的容积为2L,4min后达到平衡,测得容器内物质由2.5mol减少至2.25mol,则HCl的平均反应速率为 0.125 mol/L∙min.
;若反应容器的容积为2L,4min后达到平衡,测得容器内物质由2.5mol减少至2.25mol,则HCl的平均反应速率为 0.125 mol/L∙min.