金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝。高温下,在密
闭容器中用H2还原WO3可得到金属钨,其总反应为:WO3 (s) + 3H2 (g)  W (s) + 3H2O (g)
W (s) + 3H2O (g)
请回答下列问题:
(1)上述反应的化学平衡常数表达式为___________________________。
(2)某温度下反应达平衡时,H2与水蒸气的体积比为3:5,则H2的平衡转化率__________________。
(3)上述总反应过程大致分为三个阶段,各阶段主要成分与温度的关系如下表所示:
| 温度 | 25℃ ~ 550℃ ~ 600℃ ~ 700℃ |
| 主要成份 | WO3 W2O5 WO2 W |
500℃时,固体物质的主要成分为 ;
第二阶段反应的化学方程式为 ;
假设WO3完全转化为W,则三个阶段消耗H2物质的量之比为________________。
钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I2可延长灯管的使用寿命,其工作 原理为:W (s) +2I2 (g)  WI4 (g)。下列说法正确的有________________
WI4 (g)。下列说法正确的有________________
a.灯管内的I2可循环使用
b.WI4在灯管壁上分解,使灯管的寿命延长
c.WI4在灯丝上分解,产生的W又沉积在灯丝上
d.接通电源后,WI4的分解速率加快,W和I2的化合速率减慢
煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程。
(1)将水蒸气通过红热的炭即可产生水煤气。反应为:C(s)+H2O(g) 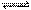 CO(g)+H2(g)
CO(g)+H2(g)
ΔH=+131.3 kJ·mol-1 一定温度下,在一个容积可变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是 (填字母,下同)
a.容器中的压强不变 b.1 mol H—H键断裂的同时断裂2 mol H—O键
c.v正(CO)=v逆(H2O) d.c(CO)=c(H2)
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2 L的恒容密闭容器中,进行反应
CO(g)+H2O(g) 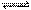 CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
| 实 验 组 | 温 度 /℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
①该反应的逆反应为________(填“吸”或“放”)热反应。
②若实验3要达到与实验2相同的平衡状态(即各物质的质量分数分别相等),且t<3 min,则a、b应满足的关系是 (用含a、b的数学式表示)。
 目前工业上有一种方法是用CO2来生产甲醇。一定条件下
目前工业上有一种方法是用CO2来生产甲醇。一定条件下
发生反应:CO2(g)+3H2(g) 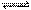 CH3OH(g)+H2O(g),如图表示 该反应进行过程中能量(单位为kJ·mol-1)的变化。在体积为1 L的恒容密闭容器中,充入1 mol CO2和3 mol H2, 下列措施中能使 c(CH3OH)增大的是
CH3OH(g)+H2O(g),如图表示 该反应进行过程中能量(单位为kJ·mol-1)的变化。在体积为1 L的恒容密闭容器中,充入1 mol CO2和3 mol H2, 下列措施中能使 c(CH3OH)增大的是
a.升高温度
b.充入N2(g),使体系压强增大
c.将H2O(g)从体系中分离出来
d.再充入0.5 mol CO2和1.5 mol H2
 H2CO3 + 2OH-
H2CO3 + 2OH-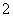 +2H2O
+2H2O AlCl3
AlCl3 Al ② NH3
Al ② NH3 NO
NO HNO3
HNO3 NaHCO3
NaHCO3 Na2CO3 ④FeS2
Na2CO3 ④FeS2 SO3
SO3 H2SO4
H2SO4




 B. Mg2+的结构示意图:
B. Mg2+的结构示意图:
 D.核内有8个中子的碳原子:
D.核内有8个中子的碳原子: C
C