某同学用如图所示的装置来探究SO2的性质。
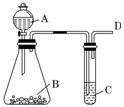
(1)实验前首先应做的操作是_________________________________________________。
(2)实验室用亚硫酸钠固体与较浓硫酸反应制取SO2气体,写出该反应的化学方程式:________________________________________________________________________。
(3)分别将SO2气体通入下列C溶液中,请回答下列问题:
 ①若C为紫色石蕊试液:
①若C为紫色石蕊试液:
| 操作 | 现象 |
| 通入少量SO2 | |
| 继续通入过量SO2 |
②若C为品红溶液:
| 操作 | 现象 |
| 通入足量SO2 | |
| 将试管加热 |
③若C为酸性KMnO4溶液,通入足量SO2,现象______________,KMnO4被________。
④若C为澄清石灰水,通入足量SO2,现象__________________,发生反应的离子方程式________________________________________________________________________
________________________________________________________________________。
某合作小组同学在进行酸性高锰酸钾溶液与草酸(化学式为H2C2O4,为弱酸,被氧化为CO2)溶液的反应时,发现刚开始一段时间,反应速率较慢,溶液褪色不明显,但不久后突然褪色,反应速率明显加快。该小组通过实验探究其原因。
(1)该反应的离子方程式为
(2)该实验中反应速率明显加快的原因可能是
A.反应放热导致温度升高 B.反应物接触面积增大
C.生成物的催化作用 D.压强增大
(3)为验证该反应速率明显加快的原因,甲同学继续进行了下列实验,请完成下表。
| 编号 | 温度/℃ | 酸化的H2C2O4溶液/mL | KMnO4溶液/mL | 溶液褪色所需时间/s |
| 1 | 25 | 5.0 | 2.0 | 40 |
| 2 | 25 | (另加少量可溶于水的MnSO4粉末) |
| 4 |
| 3 | 60 |
|
| 25 |
(4)已知25℃时,c(H2C2O4)~反应时间t的变化曲线如图,若保持其他条件不变,画出加入催化剂时c(H2C2O4)~反应时间t的变化曲线示意图(进行相应的标注)。

 用图所示实验装置(夹持仪器已略去)探究铜丝与
用图所示实验装置(夹持仪器已略去)探究铜丝与 色
色 3SO2↑+2H2O,在此反应中,浓硫酸既表现了其强氧化性又表现了其酸性
3SO2↑+2H2O,在此反应中,浓硫酸既表现了其强氧化性又表现了其酸性
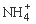 和NH3·H2O的形式存在,该废水的处理流程如下:
和NH3·H2O的形式存在,该废水的处理流程如下: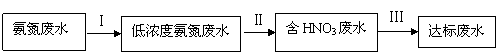

 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:

 +4H+=PbSO4+2H2O,则在a电极上发生的反应可表示为_________________。若电池工作一段时间后,a极消耗0.05 mol Pb,则W的浓度由质量分数39 % (密度1.3 g/cm3)变为_____ _mol/L。(计算结果保留两位小数)
+4H+=PbSO4+2H2O,则在a电极上发生的反应可表示为_________________。若电池工作一段时间后,a极消耗0.05 mol Pb,则W的浓度由质量分数39 % (密度1.3 g/cm3)变为_____ _mol/L。(计算结果保留两位小数)


