元素周期表是学习物质结构与性质的重要工具。下表是元素周期表的一部分,表中所列字母A、B、D、E、G、H、Q、M、R分别代表某一化学元素。请用所给元素回答下列问题。
| A | |||||||||||||||||
| M | B | D |
| ||||||||||||||
| G | H |
|
| Q | R | ||||||||||||
| E |
| ||||||||||||||||
(1)Q元素在元素周期表中的位置 ,E元素原子结构示意图为
(2)E、Q、R三种元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是(填离子符号)_________________________________。
(3)M、D两元素形成的化合物中含有的化学键类型是 ,其MD2分子的结构式:
(4)用电子式表示物质GDA_________________; 用电子式表示G与Q形成化合物的过程 ;
(5)用表中所给元素组成反应物,请各用一个化学方程式说明元素Q和R非金属性的强弱: ;元素G、H的金属性强弱:
 NA个NO分子
NA个NO分子 氧化成
氧化成 ,而稀硝酸不能氧化
,而稀硝酸不能氧化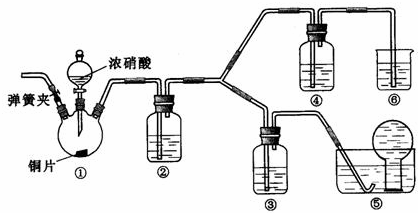

 材料2:Cu+在酸性溶液中不稳定,可发生自身氧化还原反应生成:Cu2+和Cu:Cu2O + 2H+ == Cu2+ + Cu +H2O
材料2:Cu+在酸性溶液中不稳定,可发生自身氧化还原反应生成:Cu2+和Cu:Cu2O + 2H+ == Cu2+ + Cu +H2O bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示: (1)此反应的化学方程式中
(1)此反应的化学方程式中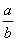 =__________
=__________ 