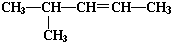0 135320 135328 135334 135338 135344 135346 135350 135356 135358 135364 135370 135374 135376 135380 135386 135388 135394 135398 135400 135404 135406 135410 135412 135414 135415 135416 135418 135419 135420 135422 135424 135428 135430 135434 135436 135440 135446 135448 135454 135458 135460 135464 135470 135476 135478 135484 135488 135490 135496 135500 135506 135514 203614

 如图有机物A的分子,所含有的官能团的名称是
如图有机物A的分子,所含有的官能团的名称是
 我国化学家在“铁基(氟掺杂镨氧铁砷化合物)高温超导”材料研究上取得了重要成果,该研究项目荣获2013年度“国家自然科学奖”一等奖.
我国化学家在“铁基(氟掺杂镨氧铁砷化合物)高温超导”材料研究上取得了重要成果,该研究项目荣获2013年度“国家自然科学奖”一等奖. 某化学小组同学向一定量加入少量淀粉的NaHSO3溶液中加入稍过量的KIO3溶液,一段时间后,溶液突然变蓝色.
某化学小组同学向一定量加入少量淀粉的NaHSO3溶液中加入稍过量的KIO3溶液,一段时间后,溶液突然变蓝色. (Ⅰ)已知:H+(aq)+OH-(aq)═H2O(l)△H1=-57.3kJ/mol
(Ⅰ)已知:H+(aq)+OH-(aq)═H2O(l)△H1=-57.3kJ/mol