0 135297 135305 135311 135315 135321 135323 135327 135333 135335 135341 135347 135351 135353 135357 135363 135365 135371 135375 135377 135381 135383 135387 135389 135391 135392 135393 135395 135396 135397 135399 135401 135405 135407 135411 135413 135417 135423 135425 135431 135435 135437 135441 135447 135453 135455 135461 135465 135467 135473 135477 135483 135491 203614
 (1)弱酸HA的电离常数 K=
(1)弱酸HA的电离常数 K=


 转变为
转变为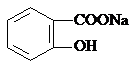 的流程为
的流程为
