 在容积为2.0L的密闭容器内,物质D在T℃时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,下列叙述不正确的是( )
在容积为2.0L的密闭容器内,物质D在T℃时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,下列叙述不正确的是( )| A、从反应开始到第一次达到平衡时,A物质的平均反应速率为0.667mol/(L?min) |
| B、该反应的化学方程式为2D(s)?2A(g)+B(g)该反应的平衡常数表达式为K=c(A)2?c(B) |
| C、已知反应的△H>0,则第5分钟时图象呈现上述变化的原因可能是升高体系的温度 |
| D、若在第7分钟时增加D的物质的量,则表示A的物质的量变化正确的是a曲线 |
气体甲通入溶液乙中时,随着甲的通入,溶液乙的颜色逐渐褪去,下列说法正确的是( )
| A、气体甲一定具有漂白性 |
| B、溶液乙褪色后,不可能再恢复原来的颜色 |
| C、气体甲一定与溶液乙中的某种有色物质发生化合反应 |
| D、气体甲可能被溶液乙中的某些离子氧化 |
铁和稀硫酸在敞口容器中进行反应:Fe+H2SO4=FeSO4+H2↑,下列叙述不正确的是( )
A、该反应的反应过程与能量关系可以用图表示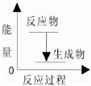 |
| B、若将该反应设计成原电池,当正极产生22.4L气体时,有56g铁溶解 |
| C、若将该反应设计成原电池,溶液中SO42-向Fe电极移动 |
| D、若将该反应设计成原电池,负极发生的反应是:Fe-2e=Fe2+ |
石灰氮是由Ca、N、C等三种元素组成的盐,其含钙、碳的质量分数分别为50%、l5%.
①石灰氮完全水解的产物是A和B,其中B可方便地制成一种氮肥;
②A在高温下分解生成C和D,通常状况下,C为气体;
③B的催化氧化产物为E和F;
④E遇到D生成唯一产物G,G与C反应重新生成A和E;
⑤F再被氧气氧化后的产物遇到E可制备常用的一种强酸H;
⑥B、C、E混合反应生成一种常用的氮肥I.
以下有关叙述中正确的是( )
①石灰氮完全水解的产物是A和B,其中B可方便地制成一种氮肥;
②A在高温下分解生成C和D,通常状况下,C为气体;
③B的催化氧化产物为E和F;
④E遇到D生成唯一产物G,G与C反应重新生成A和E;
⑤F再被氧气氧化后的产物遇到E可制备常用的一种强酸H;
⑥B、C、E混合反应生成一种常用的氮肥I.
以下有关叙述中正确的是( )
| A、石灰氮是化学式为Ca(CN)2 |
| B、②、⑤、⑥为有关工业生产过程的反应原理 |
| C、1mol B经过催化氧化生成E和F的过程中有3mol电子发生转移 |
| D、足量B和C与饱和氯化钠溶液反应可以制得发酵粉的一种主要成分 |
将含有0.1mol明矾[KAl(SO4)2?12H2O]的溶液和100mL 2mol?L-1的Ba(OH)2溶液混合后,下列叙述正确的是( )
| A、反应完毕后,液体仍然澄清 |
| B、溶液浑浊,沉淀物是BaSO4 |
| C、生成0.1mol Al(OH)3和0.2mol BaSO4 |
| D、溶液浑浊,沉淀物是Al(OH)3 |
某气态烃1mol与2mol HCl发生加成反应,所得的加成产物每摩又能与8mol氯气反应,最后得到一种只含碳、氯元素的化合物,则气态烃为( )
| A、丙炔 | B、1,3-丁二烯 |
| C、1-丁烯 | D、丙烯 |
下列说法中不正确的是( )
| A、蒸馏是分离提纯相互互溶的液态有机物的常用方法 |
| B、石油分馏可获得乙烯、丙烯和丁二烯 |
| C、通过煤的直接或间接液化,可以获得燃料油及多种化工原料 |
| D、重结晶法提纯苯甲酸时,杂质的溶解度很小或很大均易于除去 |
类推的思维方式在化学学习与研究中经常采用,但类推出的结论是否正确最终要经过实践的验证.以下类推的结论正确的是( )
| A、不能用电解AlCl3来制取Al,也不能用电解MgCl2来制取镁 |
| B、金刚石的硬度大,则C60的硬度也大 |
| C、CO2与SiO2化学式相似,则CO2与SiO2的物理性质也相似 |
| D、Na、K在周期表中属于同一主族,化学性质相似,Na常温下与水剧烈反应,故K常温下也能与水剧烈反应 |
一定条件下体积为10L的密闭容器中,1mol X和1mol Y进行反应:2X(g)+Y(g)?Z(g),60s时达到平衡,生成0.3mol Z.下列说法正确的是( )
| A、反应进行30s时,正反应速率等于逆反应速率 |
| B、反应进行80s时,逆反应速率大于正反应速率 |
| C、这段时间内以X的浓度变化表示的反应速率为0.001mol/(L?s) |
| D、反应进行80s时,X物质的量浓度为0.4mol/L |
