将质量为w1 g的钠、铝混合物投入一定量的水中充分反应,金属没有剩余,共收集到标准状况下的气体V1 L.向溶液中逐渐加入浓度为a mol/L的HCl溶液,反应过程中先有白色沉淀生成后又逐渐溶解,当沉淀恰好消失时所加HCl溶液体积为V2 L.将溶液蒸干灼烧得固体w2 g.下列关系式中正确的是( )
A、n(Na)+3n(Al)=
| ||
B、aV2=
| ||
| C、35.5aV2=w2-w1 | ||
| D、35.5aV2>(w2-w1) |
已知氧化性:Br2>Fe3+>I2,向含有a mol FeI2的溶液中加入含b mol Br2的溴水,下列判断或相应的离子方程式正确的是( )
| A、当a=2,b=1时,离子方程式为:2Fe2++Br2→2Fe3++2Br- | ||||
B、如果反应后的溶液中存在c(Fe2+)=c(Fe3+),则
| ||||
| C、当a=1,b=2时,离子方程式为:2Fe2++4I-+3Br2→2Fe3++2I2+6Br- | ||||
| D、当a=2,2<b<3时,溶液中铁元素以两种离子形式存在,且一定是c(Fe3+)>c(Fe2+) |
下列叙述中正确的是( )
| A、摩尔物质约含有6.02×1023个构成这种物质的微粒 |
| B、氧气的摩尔质量是32g |
| C、1mol任何气体的气体摩尔体积都约是22.4L?mol-1 |
| D、1mol?L-1硫酸溶液的含义是指1L水中含有lmol硫酸 |
下列实验与对应的图象符合的是( )
A、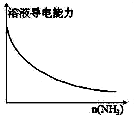 向一定量的CH3COOH溶液中通入NH3至过量 |
B、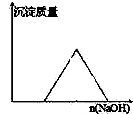 向等物质的量的HCl和AlCl3溶液中滴入NaOH溶液至过量 |
C、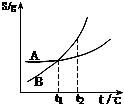 表示A、B两物质的溶解度随温度变化情况,将t1℃时A、B饱和溶液升温至t2℃时,溶质的质量分数B=A |
D、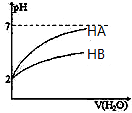 表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH大于NaB溶液 |
“可燃冰”是水与天然气相互作用形成的晶体物质,经研究测定:每立方米“可燃冰”可释放出200m3的甲烷气体.下列说法不正确的是( )
| A、“可燃冰”将有可能成为新能源 |
| B、“可燃冰”实质是水变成的固态油 |
| C、“可燃冰”使用方便,清洁卫生 |
| D、在海底和冻土层可能存在“可燃冰” |
关于SO2的叙述错误的是( )
| A、不能形成酸雨 |
| B、密度比空气的大 |
| C、不能与浓硫酸反应 |
| D、能使品红溶液褪色 |
某研究小组利用“钯催化交叉偶联反应”合成了有机物丙,合成路线如下:

下列分析判断正确的是( )

下列分析判断正确的是( )
| A、分离提纯有机物丙宜在NaOH热溶液中进行 |
| B、利用NaOH溶液、AgNO3溶液即可确定有机物甲中含有溴元素 |
| C、可用酸性KMnO4溶液检验有机物丙中是否含有机物乙 |
| D、PbCl2的作用是提高反应物的活性,加快反应速率 |
短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13.X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍也是Y原子最外层电子数的3倍.下列说法正确的是( )
| A、Y与Z形成的简单离子核外电子排布相同 |
| B、X的氧化物为离子化合物 |
| C、Z的氢化物的水溶液在空气中容易变质 |
| D、X与Z对应的氧化物的水化物一定为强酸 |
下列对淀粉、纤维素的叙述正确的是( )
| A、它们的组成都是(C6H10O5)n,但n值不同,因此淀粉、纤维素互为同系物 |
| B、它们都不溶于水,在热水中颗粒会膨胀破裂,发生酯化作用 |
| C、它们都属于高分子化合物,一定条件下都可以水解,最终产物都是葡萄糖 |
| D、淀粉是还原性糖,纤维素是非还原性糖 |
可以使湿润的红色石蕊试纸变蓝的气体是( )
| A、NO |
| B、HCl |
| C、NH3 |
| D、NO2 |