下列离子方程式正确的是( )
| A、实验室中制取CO2:CO32-+2H+═CO2↑+H2O |
| B、钠投入CuSO4溶液中:2Na+Cu2++2H2O═2Na++Cu(OH)2↓+H2↑ |
| C、向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O═HClO+HSO3- |
| D、向酸性KMnO4溶液中滴加双氧水:2MnO4-+H2O2+6H+═2Mn2++3O2↑+4H2O |
对实验A-D的实验现象预测正确的是( )
A、 试管中红色溶液逐渐变成无色溶液 |
B、 试管中出现淡黄色浑浊 |
C、 铁棒上有无色气泡产生 |
D、 酸性KMnO4溶液中出现气泡且颜色逐渐褪去 |
碱性电池具有容量大、放电电流大的特点,因此得到广泛的应用.锌锰碱性电池以氢氧化钾溶液为电解液,电池总反应为Zn(s)+2MnO2(s)+H2O═Zn(OH)2(s)+Mn2O3(s),下列说法错误的是( )
| A、电池工作时,锌失去电子 |
| B、电池负极的电极反应式为:Zn-2e-+2OH-═Zn(OH)2 |
| C、电池工作时,电子由正极通外电路流向负极 |
| D、外电路中每通过0.2mol电子,锌的质量理论上减小6.5g |
用1L 1.0mol?L-1的NaOH溶液吸收0.6mol CO2,所得溶液中的CO32-和HCO3-的物质的量浓度之比约是( )
| A、1:3 | B、2:1 |
| C、2:3 | D、3:2 |
关于下列各图的叙述正确的是( )
A、 表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6kJ?mol-1 |
B、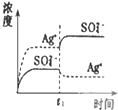 表示向Ag2SO4饱和溶液中加入等体积Na2SO4稀溶液,平衡会向左移动,Ksp减小 |
C、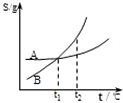 表示A、B两物质的溶解度随温度变化情况,将A、B饱和溶液分别由t1℃升温至t2℃时,溶质的质量分数B>A |
D、 表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB溶液 |
“神舟六号”用动力燃料之一为氢化锂三兄弟--LiH、LiD、LiT.其中Li的质量数为7,有关下列叙述中正确的是( )
| A、三种物质质子数之比为1:2:3 |
| B、三种物质中子数之比为0:1:2 |
| C、三种物质的摩尔质量之比为4:5:6 |
| D、三种物质核外电子数之比为1:1:1 |
下列说法正确的是( )
| A、煤中含有苯和甲苯,可用分馏的方法把它们分离出来 |
| B、C7H16的烷烃中,含有3个甲基的同分异构体有2种 |
| C、碳原子数小于或等于8的单烯烃中,与HBr加成产物只有一种结构,符合条件的单烯烃有6种 |
| D、某烃的分子式为C10H14,它不能使溴水褪色,但可使酸性KMnO4溶液褪色,且分子结构中只有一个烷基,符合条件的烃有3种 |
在一定温度下,向容积固定不变的密闭容器中充入a mol A,发生反应:2A(g)?B(g);△H<0.达平衡后再向容器中充入a mol A,再次达到平衡后,与原平衡比较,下列叙述不正确的是( )
| A、相对平均分子质量增大 |
| B、A的转化率提高 |
| C、A的质量分数增大 |
| D、反应放出的总热量大于原来的2倍 |
对以下化学问题的解释中错误的是( )
| A、工业盐酸显黄色,是由于含有杂质FeCl3 |
| B、碘化钾溶液久置显黄色,是由于I被氧化,析出的I2溶于溶液中 |
| C、浓硝酸显黄色,是由于硝酸见光分解生成的NO2溶液酸液中 |
| D、炼钢是在高温下利用还原剂除去生铁中的杂质 |
某溶液中含有下列六种离子:①HCO3-②SO32-③Na+④CO32-⑤NH4+⑥NO3-⑦SO42-向其中加入一定量Na2O2后,溶液中离子浓度基本保持不变的是( )
| A、①②⑤⑥ | B、③④⑤⑦ |
| C、②④⑦⑥ | D、只有⑥ |