0 134788 134796 134802 134806 134812 134814 134818 134824 134826 134832 134838 134842 134844 134848 134854 134856 134862 134866 134868 134872 134874 134878 134880 134882 134883 134884 134886 134887 134888 134890 134892 134896 134898 134902 134904 134908 134914 134916 134922 134926 134928 134932 134938 134944 134946 134952 134956 134958 134964 134968 134974 134982 203614

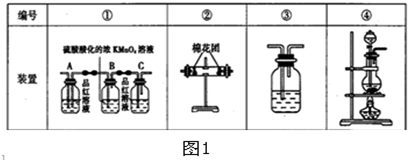
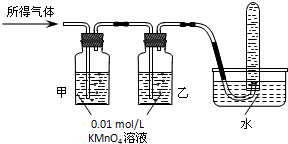



 某校高三同学高考前重做以下两个课本实验,请你回答实验过程中的相关问题:
某校高三同学高考前重做以下两个课本实验,请你回答实验过程中的相关问题:
 (-R1、-R2表示氢原子或烃基)
(-R1、-R2表示氢原子或烃基)