设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A、常温下,23g NO2含有氧原子的数目为NA |
| B、1.00mol?L-1 NaCl溶液中含有Na+的数目为NA |
| C、标准状况下,39g苯中含有的碳碳双键数为1.5NA |
| D、常温常压下,22.4L乙烯中含C-H键的数目为4NA |
以下实验能获得成功的是( )
| A、要检验某溴乙烷中的溴元素,可以加入NaOH溶液共热,冷却后滴入AgNO3溶液,观察有无浅黄色沉淀生成 |
| B、用氨水清洗试管壁附着的银镜 |
| C、对苯和硝基苯采用分液的方法分离 |
| D、将铜丝在酒精灯上加热变黑后,立即伸入无水乙醇中,铜丝恢复成原来的红色 |
钠硫高能蓄电池的结构如右下图,M为Na2O和Al2O3的混合物,电池的反应原理为2Na+xS?Na2Sx,电池工作温度为320℃.下列说法错误的是( )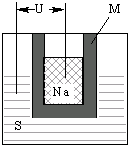

| A、Na电极为电池负极,S电极为电池正极 | ||
B、电池放电时,正极反应为xS+2e-═S
| ||
| C、电池充电时.Na所在电极连接电源正极 | ||
| D、M的作用为导电和隔离钠和硫 |
分子式为C5H11Cl的有机物分子中,所含的甲基数不可能为( )
| A、1 | B、2 | C、3 | D、4 |
关于如图中四个图象的说法正确的是( )

| A、①表示反应H2(g)+Cl2(g)=2HCl(g)能量变化,则该反应热△H=183 kJ/mol |
| B、②条件不变时,4A(g)+3B(g)?2C(g)+6D,不同压强 B% 随时间变化,则D一定是气体 |
| C、③表示10 mL 0.1mol/L Na2CO3和NaHCO3两种溶液中,分别滴加0.1mol/L HCl,产生CO2的体积随盐酸体积的变化,则b表示Na2CO3溶液 |
| D、④绝热恒容密闭容器,SO2(g)+NO2(g)?SO3(g)+NO(g)达平衡,结论是,△t1=△t2时,SO2的转化率:a---b段小于b---c段 |
可用如图所示玻璃试剂瓶(带玻璃塞)长期盛放的试剂是( )


| A、浓硫酸 | B、饱和碳酸钠溶液 |
| C、氢氟酸 | D、氢氧化钠溶液 |
在0.1mol/L的醋酸溶液中存在如下电离平衡:CH3COOH?CH3COO-+H+,对于该平衡,下列说法正确的是( )
A、加入水稀释
| ||
| B、加水稀释,醋酸的电离度虽然增大,但溶液中各种离子的浓度均减小 | ||
| C、因为醋酸钠水解显碱性,故加入少量的醋酸钠固体,平衡向电离方向移动 | ||
| D、该溶液pH增大时,CH3COO-浓度也增大 |
下列有关实验原理或操作正确的是( )
| A、为除去苯中的少量苯酚,向混合物中加入适量的溴水后过滤 |
| B、制备乙酸乙酯时,向乙醇中缓慢加入浓硫酸和冰醋酸 |
| C、用粥汤检验加碘盐中是否含碘 |
| D、在苯萃取溴水中的溴,分液时有机层从分液漏斗的下端放出 |
在下列叙述中,能说明盐酸是强酸,醋酸是弱酸的是( )
| A、将等体积pH=4的盐酸和醋酸稀释到pH=5的溶液,醋酸所加的水量少 |
| B、盐酸可与醋酸钠溶液反应生成醋酸 |
| C、相同pH的盐酸和醋酸分别跟锌反应时,产生氢气的起始速率相等 |
| D、等体积、相同pH的盐酸和醋酸溶液中分别加入相应的钠盐固体,醋酸pH变大 |
英国科学家近日研发出一种名为NOTT-202a的新型多孔材料,空气中其他气体可自由通过这些孔洞,但CO2会被截留.该材料的分子结构单元是以铟原子为中心,周围是以各种有机分子链条编织成的“笼子”,整体上看呈现出多孔特征,有些类似自然界中的蜂窝结构.下列有关说法正确的是( ) 

| A、该材料是一种特殊结构的金属 |
| B、该材料只吸收CO2,其他任何气体都能自由通过 |
| C、该材料吸收22.4LCO2后,增重44g |
| D、该材料可用于工厂的烟囱,吸收CO2,减少碳排放 |