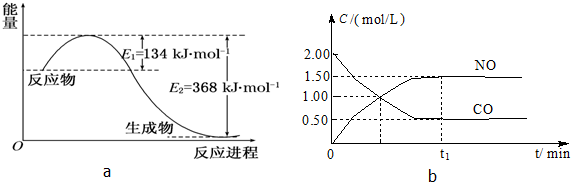
下列有关说法正确的是( )
| A、反应NH3(g)+HCl(g)═NH4Cl(s)在室温下可自发进行,则该反应的△H<0 |
| B、当镀锡铁和镀锌铁镀层破损时,后者更易被腐蚀 |
| C、CH3COOH溶液加水稀释后,电离平衡正向移动,溶液中的c(CH3COO-)增大 |
| D、Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH减小 |
已知反应A2+B2=2AB,断开1molA2中的化学键消耗的能量为Q1 kJ,断开1molB2中的化学键消耗的能量为Q2kJ,生成1molAB中的化学键释放的能量为Q3kJ,则下列说法正确的是( )
| A、若A2和B2的总能量之和大于生成的2AB的总能量,则反应放热 |
| B、若A2和B2的总能量之和小于生成的2AB的总能量,则反应放热 |
| C、若该反应为放热反应,则Q1+Q2>Q3 |
| D、若该反应为吸热反应,则Q1+Q2<Q3 |
下列说法或表示法正确的是( )
| A、等量的硫蒸汽和硫固体分别完全燃烧,后者放出热量多 |
| B、在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)═2H2O(l);△H=-285.8kJ/mol |
| C、在稀溶液中:H+(aq)+OH-(aq)═H2O(l);△H=-57.3kJ/mol,则稀醋酸溶液与稀氢氧化钠溶液混合,中和热仍为57.3kJ/mol |
| D、由C(石墨)→C(金刚石):△H=+119kJ/mol可知,石墨比金刚石稳定 |
下列说法不正确的是( )
| A、一个反应能否自发进行取决于该反应放热还是吸热 |
| B、同一条件下不同物质有不同的熵值,其体系的混乱程度越大,熵值越大 |
| C、焓变是一个与反应能否自发进行有关的因素,多数能自发进行的反应都是放热反应 |
| D、一个反应能否自发进行,与焓变和熵变的共同影响有关 |
下列说法正确的是( )
| A、需要加热才能发生的反应一定是吸热反应 |
| B、反应物和生成物各自具有的总能量决定反应是放热还是吸热 |
| C、任何放热反应在常温条件下一定能发生 |
| D、镁和氧气反应生成氧化镁后,生成物能量明显升高 |
下列说法中,正确的是( )
| A、铜锌原电池中,电子由锌极经导线流向铜极 |
| B、铜锌原电池中,锌作阳极,铜作阴极 |
| C、石墨电极电解氯化铜溶液的反应中,阳极上质量增重 |
| D、石墨电极电解氯化钠溶液的反应中,用氢氧化钠溶液吸收阴极产物 |
LiFePO4电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车.电池反应为:FePO4+Li
LiFePO4,含Li+导电固体为电解质.下列有关LiFePO4电池说法不正确的是( )
| 放电 |
| 充电 |
| A、可加入硫酸以提高电解质的导电性 |
| B、充电时LiFePO4既发生氧化反应又发生还原反应 |
| C、充电过程中,电池正极材料的质量减少 |
| D、放电时电池正极反应为:FePO4+Li++e-═LiFePO4 |