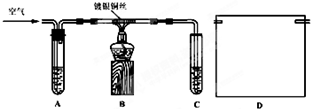
aX(g)+bY(g)?cZ(g)+dW(g)在一定容积的密闭容器中反应,5min时达到平衡,X减少 n mol?L-1,Y减少
mol?L-1,Z增加
mol?L-1.若将体系压强增大,W的百分含量不发生变化.则化学方程式中各物质的化学计量数之比a:b:c:d应为( )
| n |
| 3 |
| 2n |
| 3 |
| A、3:1:2:1 |
| B、1:3:2:2 |
| C、1:3:1:2 |
| D、3:1:2:2 |
将KCl和KBr的混合物26.8g溶于水配成500mL溶液,通入过量的Cl2.反应后将溶液蒸干,得固体22.35g,则原溶液中K+、Cl-、Br-的物质的量之比是( )
| A、3:2:1 |
| B、4:3:1 |
| C、5:2:3 |
| D、5:4:1 |
一定条件下,若 N2、H2、NH3起始浓度分别为c1、c2、c3(均不为0),当达平衡时N2、H2、NH3的浓度分别为0.1mol/L,0.3mol/L,0.08mol/L,则下列判断不合理的是( )
| A、c1:c2=1:3 |
| B、N2、H2的转化率不相等 |
| C、平衡时,H2和NH3的生成速率之比为3:2 |
| D、c1的取值范围为0<c1<0.14 mol/L |
在恒容的密闭容器中加入1mol N2和3mol H2发生反应:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1,下列有关说法正确的是( )
| A、平衡前,随着反应的进行,容器内气体密度逐渐减小 |
| B、平衡时,若断裂π键0.4 mol,则放出的热量为18.48 kJ |
| C、平衡后,再向容器中通入1 mol氦气,H2的转化率增大 |
| D、平衡后,缩小容器体积,N2的浓度减小 |
一块钠久置后变质为1.55g钠、氧化钠、过氧化钠的混合物,将此混合物用足量的水溶解后,产生标况下气体336mL,在所得溶液中加入50mL、1mol/L的盐酸,恰呈中性.则原钠块的质量为( )
| A、0.92g |
| B、1.07g |
| C、1.15g |
| D、1.23g |
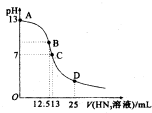 氮气是空气中含量最多的一种气体,氮气及其化合物在工农业生产、生活中有着广泛的应用.请回答下列问题:
氮气是空气中含量最多的一种气体,氮气及其化合物在工农业生产、生活中有着广泛的应用.请回答下列问题: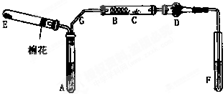 如图是某化学兴趣小组设计的乙醇催化氧化的实验装置(图中加热仪器、铁架台、试管夹均未画出).图中A处为无水乙醇(沸点78℃),B处为绕成螺旋状的细铜丝或银丝,C处为无水CuSO4粉末,D处为碱石灰,F处为新制的碱性Cu(OH)2悬浊液.
如图是某化学兴趣小组设计的乙醇催化氧化的实验装置(图中加热仪器、铁架台、试管夹均未画出).图中A处为无水乙醇(沸点78℃),B处为绕成螺旋状的细铜丝或银丝,C处为无水CuSO4粉末,D处为碱石灰,F处为新制的碱性Cu(OH)2悬浊液.