 实验室常用如图所示装置测定某固体有机物A的分子组成,测定装置如图(铁架台、铁夹、酒精灯等未画出).下列说法正确的是( )
实验室常用如图所示装置测定某固体有机物A的分子组成,测定装置如图(铁架台、铁夹、酒精灯等未画出).下列说法正确的是( )| A、测定前要先通入纯氧气,再点燃试管B |
| B、装置C可测定有机物中碳的含量 |
| C、装置D可测定燃烧产物中水的质量 |
| D、该装置能测定所有有机物的分子组成 |
已知异戊烷和新戊烷的燃烧热如下表,下列有关说法中正确的是( )
| 物质 | 异戊烷 | 新戊烷 |
| 燃烧热(kJ?mol-1) | 3504.1 | 3501.6 |
| A、异戊烷燃烧的热化学方程式为(CH3)2CHCH2CH3(l)+8O2(g)═5CO2(g)+6H2O(g)△H=-3504.1 kJ?mol-1 |
| B、C(CH3)4(g)+8O2(g)═5CO2(g)+6H2O(l)△H=+3501.6 kJ?mol-1 |
| C、(CH3)2CHCH2CH3(l)═C(CH3)4(l)△H=-2.5 kJ?mol-1 |
| D、稳定性:异戊烷>新戊烷 |
组成晶体的质点(分子、原子、离子)以确定的位置在空间作有规则排列,具有一定几何形状的空间格子,称为晶格,晶格中能代表晶体结构特征的最小重复单位称为晶胞.在冰晶石(Na3AlF6)晶胞中,AlF63-占据的位置相当于NaCl晶胞中C1-占据的位置,则冰晶石晶胞中含有的原子数与食盐晶胞中含有的原子数之比为( )
| A、2:1 | B、3:2 |
| C、5:2 | D、5:1 |
下列说法正确的是( )
A、钾(K)原子基态的原子结构示意图为 |
B、H2O电子式为 |
| C、Mg的原子基态电子排布式为1s22s22p63s23p1 |
| D、Ca2+离子基态电子排布式为1s22s22p63s23p6 |
 向某恒容密闭容器中充入一定量CO2和H2,发生反应:CO2(g)+H2(g)?HCOOH(g),测得体系中CO2的百分含量(CO2%)与反应温度变化的关系如图所示.下列物理量中,a点大于b点的是( )
向某恒容密闭容器中充入一定量CO2和H2,发生反应:CO2(g)+H2(g)?HCOOH(g),测得体系中CO2的百分含量(CO2%)与反应温度变化的关系如图所示.下列物理量中,a点大于b点的是( )| A、反应速率 |
| B、体系压强 |
| C、HCOOH(g)的浓度 |
| D、对应温度时的平衡常数 |
有a,b,c,d四种可溶性盐的溶液,它们的阳离子可能是Ba2+,Ag+,Na+,Cu2+中的一种,阴离子可能是NO3-,SO42-;Cl-,SO32-离子中的一种,做如下实验,现象如下:
(1)若把四种盐分别溶于水中,只见c盐溶液呈蓝色;
(2)若向(1)的四种盐溶液中分别加入HCl时,d盐溶液中有刺激性气味的气体逸出,
则a,b,c,d分别是( )
(1)若把四种盐分别溶于水中,只见c盐溶液呈蓝色;
(2)若向(1)的四种盐溶液中分别加入HCl时,d盐溶液中有刺激性气味的气体逸出,
则a,b,c,d分别是( )
| A、NaCl AgNO3 CuSO4 BaSO4 |
| B、BaCl2 AgNO3 CuSO4 Na2SO3 |
| C、Ba(NO3)2 Ag2SO4 CuCl2 Na2SO3 |
| D、Ag2SO4 Ba(NO3)2 CuCl2 Na2SO3 |
某无色混合气体,可能含有CO、H2、SO2、Cl2、HCl中的一种或几种,把它们通过NaOH溶液,无明显现象;再通过红热的CuO粉末,粉末变成红色;最后通往AgNO3溶液中,无沉淀生成,原混合气体中( )
| A、肯定没有Cl2和HCl |
| B、CO和H2中至少有一种 |
| C、不能确定有无HCl、SO2 |
| D、肯定有SO2 |
下列实验设计和结论相符的是( )
| A、将碘水倒入分液漏斗中,加适量乙醇,振荡后静置、分液,从而分离碘和水 |
| B、某气体能使湿润的蓝色石蕊试纸变红,该气体一定是酸 |
| C、向某无色溶液中加入AgNO3溶液,再加入稀硝酸,白色沉淀不溶解,则原溶液中一定有Cl- |
| D、向含FeCl2杂质的FeCl3溶液中通入足量Cl2后,充分加热煮沸,除去过量的Cl2,即可得到较纯净的FeCl3溶液 |
实验是研究化学的基础,下图中所示的实验方法、装置或操作均正确的是( )
A、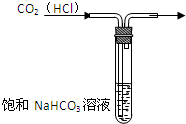 除去混有的杂质气体 |
B、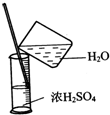 浓硫酸稀释 |
C、 分离出AgNO3溶液中的AgCl |
D、 称量30.46g的NaOH固体 |