0 125558 125566 125572 125576 125582 125584 125588 125594 125596 125602 125608 125612 125614 125618 125624 125626 125632 125636 125638 125642 125644 125648 125650 125652 125653 125654 125656 125657 125658 125660 125662 125666 125668 125672 125674 125678 125684 125686 125692 125696 125698 125702 125708 125714 125716 125722 125726 125728 125734 125738 125744 125752 203614





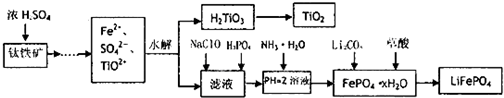


 镁是海水中含量较多的金属,镁、镁合金及其镁的化合物在科学研究和工业生产中用途非常广泛.
镁是海水中含量较多的金属,镁、镁合金及其镁的化合物在科学研究和工业生产中用途非常广泛. ,它可发生如下反应:
,它可发生如下反应: