0 125250 125258 125264 125268 125274 125276 125280 125286 125288 125294 125300 125304 125306 125310 125316 125318 125324 125328 125330 125334 125336 125340 125342 125344 125345 125346 125348 125349 125350 125352 125354 125358 125360 125364 125366 125370 125376 125378 125384 125388 125390 125394 125400 125406 125408 125414 125418 125420 125426 125430 125436 125444 203614

 Fe(SCN)3
Fe(SCN)3 CH3OH(g) △H1=-90.7 kJ·mol-1
CH3OH(g) △H1=-90.7 kJ·mol-1 CH3OCH3(g)+CO2(g)的△H= kJ·mol-1。
CH3OCH3(g)+CO2(g)的△H= kJ·mol-1。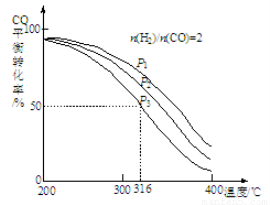

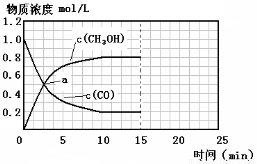
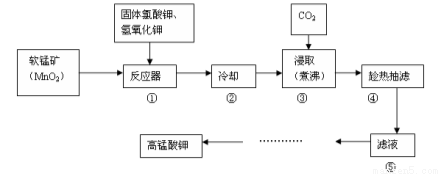



 转化为
转化为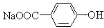 的方法是加入足量的NaOH溶液并加热, 再通入足量的CO2
的方法是加入足量的NaOH溶液并加热, 再通入足量的CO2 ,通过消去反应脱去1 molHCl时,能得到 5 种不同产物(不考虑立体异构)
,通过消去反应脱去1 molHCl时,能得到 5 种不同产物(不考虑立体异构)