0 110427 110435 110441 110445 110451 110453 110457 110463 110465 110471 110477 110481 110483 110487 110493 110495 110501 110505 110507 110511 110513 110517 110519 110521 110522 110523 110525 110526 110527 110529 110531 110535 110537 110541 110543 110547 110553 110555 110561 110565 110567 110571 110577 110583 110585 110591 110595 110597 110603 110607 110613 110621 203614
 CO2(g)+H2(g)。一段时间后该反应达到平衡,测得CO的物质的量为0.5 mol。则下列说法正确的是
CO2(g)+H2(g)。一段时间后该反应达到平衡,测得CO的物质的量为0.5 mol。则下列说法正确的是 (3)已知一氧化碳与水蒸气的反应为:CO(g)+H2O(g) CO2(g)+H2(g)
(3)已知一氧化碳与水蒸气的反应为:CO(g)+H2O(g) CO2(g)+H2(g) CO2(g)+H2(g),一段时间后反应达到平衡。对该平衡状态描述正确的是
CO2(g)+H2(g),一段时间后反应达到平衡。对该平衡状态描述正确的是 bN(g),M、N的物质的量随时间的变化曲线如图所示:
bN(g),M、N的物质的量随时间的变化曲线如图所示: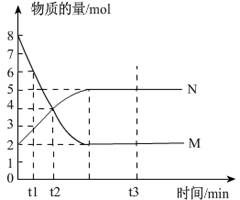
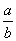 =__________
=__________ 2SO3(g);ΔH<0。向甲容器中充入1molSO2和0.5molO2,向相同容积的乙容器中充入1molSO3。若甲容器保持容积不变,乙容器保持压强不变,分别达平衡,下列说法不正确的是:
2SO3(g);ΔH<0。向甲容器中充入1molSO2和0.5molO2,向相同容积的乙容器中充入1molSO3。若甲容器保持容积不变,乙容器保持压强不变,分别达平衡,下列说法不正确的是: