0 109223 109231 109237 109241 109247 109249 109253 109259 109261 109267 109273 109277 109279 109283 109289 109291 109297 109301 109303 109307 109309 109313 109315 109317 109318 109319 109321 109322 109323 109325 109327 109331 109333 109337 109339 109343 109349 109351 109357 109361 109363 109367 109373 109379 109381 109387 109391 109393 109399 109403 109409 109417 203614

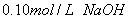 溶液,将其中一份放在空气中一段时间后,溶液的pH (填“增大”“减小”或“不变”)其原因是 。用已知浓度的盐酸中和上述两份溶液。若中和放在空气中一段时间后的那份溶液消耗盐酸的体积为
溶液,将其中一份放在空气中一段时间后,溶液的pH (填“增大”“减小”或“不变”)其原因是 。用已知浓度的盐酸中和上述两份溶液。若中和放在空气中一段时间后的那份溶液消耗盐酸的体积为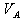 ,中和另一份溶液消耗盐酸的体积为
,中和另一份溶液消耗盐酸的体积为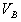 ,则(1)以甲基橙为指示剂
,则(1)以甲基橙为指示剂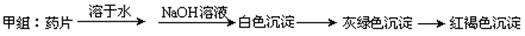 甲组同学按照设计的方案完成实验,但遗憾的是他们没有得到预期的实验结果,
甲组同学按照设计的方案完成实验,但遗憾的是他们没有得到预期的实验结果, 
 进行实验验证:________________________________
进行实验验证:________________________________ ③中溶液25.00ml,加入适量0.1%的A溶液作指示剂,立即用浓度为0.002000mol/L的硫代硫酸钠溶液滴定,并记录消耗硫代硫酸钠溶液的体积;
③中溶液25.00ml,加入适量0.1%的A溶液作指示剂,立即用浓度为0.002000mol/L的硫代硫酸钠溶液滴定,并记录消耗硫代硫酸钠溶液的体积;