0 109082 109090 109096 109100 109106 109108 109112 109118 109120 109126 109132 109136 109138 109142 109148 109150 109156 109160 109162 109166 109168 109172 109174 109176 109177 109178 109180 109181 109182 109184 109186 109190 109192 109196 109198 109202 109208 109210 109216 109220 109222 109226 109232 109238 109240 109246 109250 109252 109258 109262 109268 109276 203614
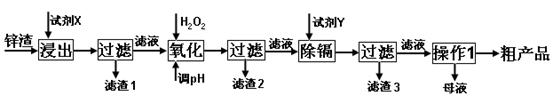



 液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填代号)_
液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填代号)_ _________。
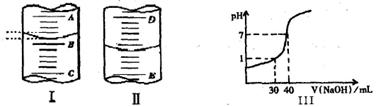
_________。
 滴定后气泡消失
滴定后气泡消失

 后,过滤;
后,过滤;

 CaCl2 + 2NH3↑+ 2H2O
CaCl2 + 2NH3↑+ 2H2O
 气泄漏事件,500 多居民深夜大转移。假如你在现场,你会采用什么自救为法? 。
气泄漏事件,500 多居民深夜大转移。假如你在现场,你会采用什么自救为法? 。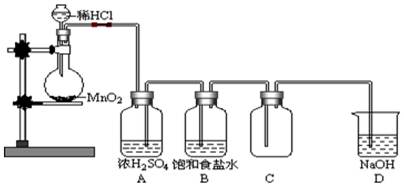
 述装置图中的错误(有几处答几处)
述装置图中的错误(有几处答几处)