0 106383 106391 106397 106401 106407 106409 106413 106419 106421 106427 106433 106437 106439 106443 106449 106451 106457 106461 106463 106467 106469 106473 106475 106477 106478 106479 106481 106482 106483 106485 106487 106491 106493 106497 106499 106503 106509 106511 106517 106521 106523 106527 106533 106539 106541 106547 106551 106553 106559 106563 106569 106577 203614

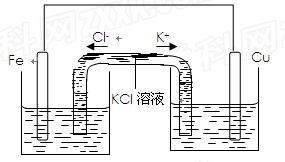


 __________。
__________。
 4NO2(g)+ O2(g)。反应5min后,测得N2O5转化了20%,则:υ(NO2)为 、5min时,N2O5占混合气体体积分数是 。
4NO2(g)+ O2(g)。反应5min后,测得N2O5转化了20%,则:υ(NO2)为 、5min时,N2O5占混合气体体积分数是 。
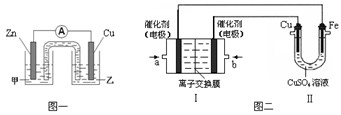
 Mx(g),反应物和生成物的物质的量随时间的变化关系如下图。下 列说法正确的是
Mx(g),反应物和生成物的物质的量随时间的变化关系如下图。下 列说法正确的是 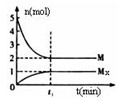
 将增大
将增大
