0 106168 106176 106182 106186 106192 106194 106198 106204 106206 106212 106218 106222 106224 106228 106234 106236 106242 106246 106248 106252 106254 106258 106260 106262 106263 106264 106266 106267 106268 106270 106272 106276 106278 106282 106284 106288 106294 106296 106302 106306 106308 106312 106318 106324 106326 106332 106336 106338 106344 106348 106354 106362 203614
 干净、干燥、称重.
干净、干燥、称重. 计算说明当充分反应
计算说明当充分反应 后铜片的质量为何值时,CH3COOAg的KSP=2.0×10-3可以得到证实.(
后铜片的质量为何值时,CH3COOAg的KSP=2.0×10-3可以得到证实.( =2.24,
=2.24,  =1.41)
=1.41) CH3COO-+H+,加水稀释后,溶液中所有离子浓度均减小;
CH3COO-+H+,加水稀释后,溶液中所有离子浓度均减小;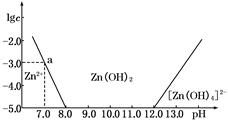
 为难溶于水和酸的白色固体,
为难溶于水和酸的白色固体, 为难溶于水和酸是黑色固体。向
为难溶于水和酸是黑色固体。向 溶液并振荡,结果白色固体完全转化为黑色固体:
溶液并振荡,结果白色固体完全转化为黑色固体: