0 106156 106164 106170 106174 106180 106182 106186 106192 106194 106200 106206 106210 106212 106216 106222 106224 106230 106234 106236 106240 106242 106246 106248 106250 106251 106252 106254 106255 106256 106258 106260 106264 106266 106270 106272 106276 106282 106284 106290 106294 106296 106300 106306 106312 106314 106320 106324 106326 106332 106336 106342 106350 203614
 PbCO3(s)+SO42—(aq)。某课题组用PbSO4为原料模拟该过程,探究上述反应的实验条件及固体产物的成分。
PbCO3(s)+SO42—(aq)。某课题组用PbSO4为原料模拟该过程,探究上述反应的实验条件及固体产物的成分。
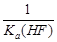

 分别在溶液中达到沉淀溶解平衡后,改变溶液
分别在溶液中达到沉淀溶解平衡后,改变溶液 ,金属阳离子浓度的辩护如图所示。据图分析,下列判断错误的是
,金属阳离子浓度的辩护如图所示。据图分析,下列判断错误的是

 固体可使溶液由
固体可使溶液由 点变到
点变到 点
点
 两点代表的溶液中
两点代表的溶液中 与
与 乘积相等
乘积相等 、
、 分别在
分别在 CH3OH(g)
CH3OH(g) 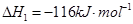
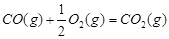
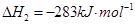
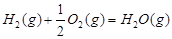
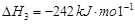
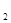 和水蒸气的热化学方程式为 。
和水蒸气的热化学方程式为 。