0 105204 105212 105218 105222 105228 105230 105234 105240 105242 105248 105254 105258 105260 105264 105270 105272 105278 105282 105284 105288 105290 105294 105296 105298 105299 105300 105302 105303 105304 105306 105308 105312 105314 105318 105320 105324 105330 105332 105338 105342 105344 105348 105354 105360 105362 105368 105372 105374 105380 105384 105390 105398 203614
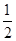 O2(g)===CO2(g)+2H2(g)ΔH=-192.9 kJ·mol-1,则CH3OH(g)的燃烧热为192.9 kJ·mol-1
O2(g)===CO2(g)+2H2(g)ΔH=-192.9 kJ·mol-1,则CH3OH(g)的燃烧热为192.9 kJ·mol-1
 2Fe(s)+3CO2(g);△H="-24.8" kJ/mol
2Fe(s)+3CO2(g);△H="-24.8" kJ/mol CO(g)
CO(g) Fe3O4(s)+
Fe3O4(s)+
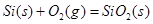 ;
;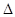 H="-989.2"
H="-989.2" 
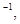 则x的值为 ( )
则x的值为 ( ) 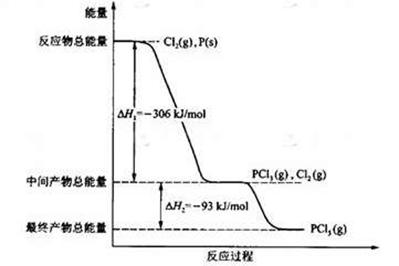
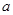 1等于 ;若反应温度由T1升高到T2,平衡时PCl5的分解率为
1等于 ;若反应温度由T1升高到T2,平衡时PCl5的分解率为