0 103311 103319 103325 103329 103335 103337 103341 103347 103349 103355 103361 103365 103367 103371 103377 103379 103385 103389 103391 103395 103397 103401 103403 103405 103406 103407 103409 103410 103411 103413 103415 103419 103421 103425 103427 103431 103437 103439 103445 103449 103451 103455 103461 103467 103469 103475 103479 103481 103487 103491 103497 103505 203614
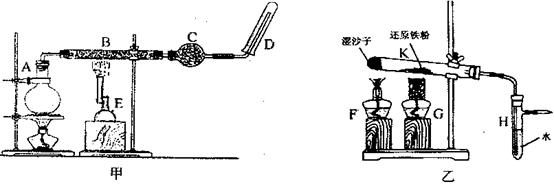
 装置的尖嘴导管处点燃反应产生的气体,装置H必不可少,H的作用是 。
装置的尖嘴导管处点燃反应产生的气体,装置H必不可少,H的作用是 。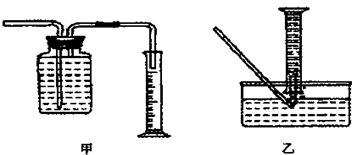
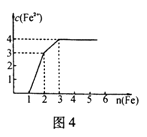
 =5.1,则被还原的硝酸的物质的量为0.1 mol
=5.1,则被还原的硝酸的物质的量为0.1 mol 2溶液中滴加稀硫酸,能使溶液变为棕黄色
2溶液中滴加稀硫酸,能使溶液变为棕黄色 硝酸铜
硝酸铜 硝酸铜
硝酸铜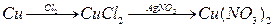
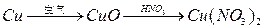

 时间置于空气中,表面“发黄”,请用化学方程式表示原因 。
时间置于空气中,表面“发黄”,请用化学方程式表示原因 。 试计算该物质沉淀完全所需要的pH= (要求保留2位有效数字)(已知溶液中离子浓度小于10-5mol/L时,该离子可看做沉淀完全,lg2=0.3)
试计算该物质沉淀完全所需要的pH= (要求保留2位有效数字)(已知溶液中离子浓度小于10-5mol/L时,该离子可看做沉淀完全,lg2=0.3)