0 103052 103060 103066 103070 103076 103078 103082 103088 103090 103096 103102 103106 103108 103112 103118 103120 103126 103130 103132 103136 103138 103142 103144 103146 103147 103148 103150 103151 103152 103154 103156 103160 103162 103166 103168 103172 103178 103180 103186 103190 103192 103196 103202 103208 103210 103216 103220 103222 103228 103232 103238 103246 203614

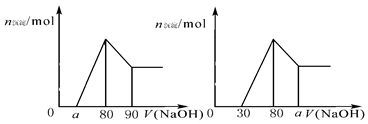
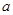 的取值范围为0≤ a<50
的取值范围为0≤ a<50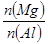 的最大值为2.5
的最大值为2.5
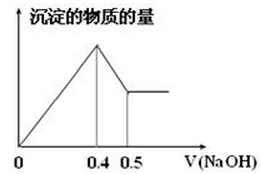
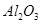 和冰晶石(
和冰晶石(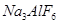 )混合熔融电解制得。
)混合熔融电解制得。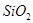 等。从铝土矿中提炼
等。从铝土矿中提炼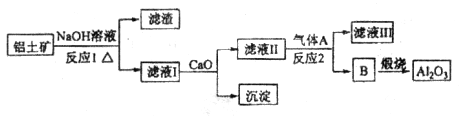
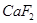 )和纯碱为原料制备冰晶石的流程如下:
)和纯碱为原料制备冰晶石的流程如下: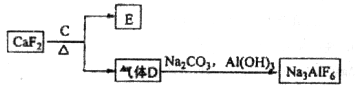
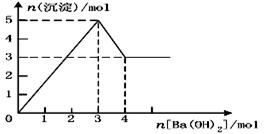
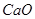 生成的沉淀是___________,反应2的离子方程式为____ ___________________
生成的沉淀是___________,反应2的离子方程式为____ ___________________