题目内容
下列图像表示Al3+与AlO2-物质的量变化的曲线,实线表示Al3+,虚线表示AlO2-,其中正确的是( )


B
试题分析:A.实线发生的反应为Al3++3OH-═Al(OH)3↓,虚线发生的反应为Al(OH)3+OH-═AlO2-+2H2O,根据原子守恒知,铝离子的最大值等于偏铝酸根离子的最大值,且第一个方程式中需要的氢氧化钠是第二个方程式的3倍,所以其纵坐标为0时,曲线拐点左右两边的氢氧化钠的物质的量之比为3:1,故A错误;B.根据A的分析知,B正确;C.向偏铝酸盐溶液中滴加盐酸先发生AlO2-+H++H2O═Al(OH)3 ↓,当沉淀最大时,继续滴加盐酸,发生反应Al(OH)3+3H+═Al3++3H2O,根据原子守恒知,偏铝酸根离子和铝离子的物质的量的最大值相等,根据方程式知,第一个方程式知盐酸的物质的量是第二个方程式的3倍,即拐点左右两边横坐标的比值为1:3,故C错误;D.根据C的分析知,故D错误;

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
 和冰晶石(
和冰晶石( )混合熔融电解制得。
)混合熔融电解制得。 等。从铝土矿中提炼
等。从铝土矿中提炼
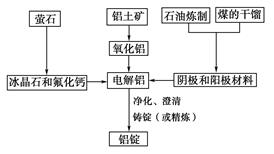
 )和纯碱为原料制备冰晶石的流程如下:
)和纯碱为原料制备冰晶石的流程如下:
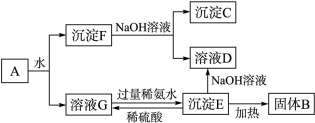
 生成的沉淀是___________,反应2的离子方程式为____ ___________________
生成的沉淀是___________,反应2的离子方程式为____ ___________________
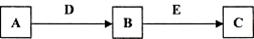

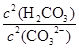 填(“变大”、“变小”或“不变”)
填(“变大”、“变小”或“不变”)