0 102261 102269 102275 102279 102285 102287 102291 102297 102299 102305 102311 102315 102317 102321 102327 102329 102335 102339 102341 102345 102347 102351 102353 102355 102356 102357 102359 102360 102361 102363 102365 102369 102371 102375 102377 102381 102387 102389 102395 102399 102401 102405 102411 102417 102419 102425 102429 102431 102437 102441 102447 102455 203614
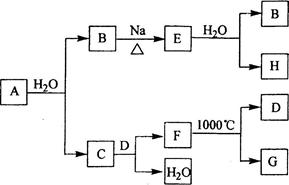
 。
。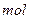 二氧化氯时,转移电子
二氧化氯时,转移电子