0 100097 100105 100111 100115 100121 100123 100127 100133 100135 100141 100147 100151 100153 100157 100163 100165 100171 100175 100177 100181 100183 100187 100189 100191 100192 100193 100195 100196 100197 100199 100201 100205 100207 100211 100213 100217 100223 100225 100231 100235 100237 100241 100247 100253 100255 100261 100265 100267 100273 100277 100283 100291 203614
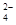 )=2:1
)=2:1