下列各组离子在指定条件下,一定能大量共存的是
A.能使蓝色石蕊试纸变红色的溶液: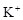 、 、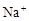 、 、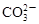 、 、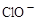 |
B.c(H+)=0.1mol·L-1的透明溶液: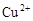 、 、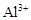 、 、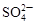 、 、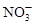 |
C.能使氢氧化铝溶解的溶液: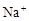 、 、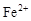 、 、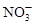 、 、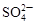 |
D.水电离出的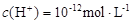 的溶液: 的溶液: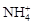 、 、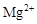 、 、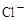 、 、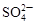 |
A.能使蓝色石蕊试纸变红色的溶液: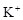 、 、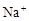 、 、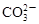 、 、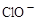 |
B.c(H+)=0.1mol·L-1的透明溶液: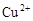 、 、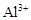 、 、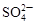 、 、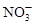 |
C.能使氢氧化铝溶解的溶液: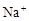 、 、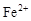 、 、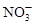 、 、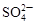 |
D.水电离出的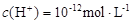 的溶液: 的溶液: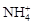 、 、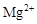 、 、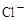 、 、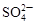 |