题目内容
9.设NA表示阿伏伽德罗常数,下列叙述中不正确的是( )| A. | 23g Na在化学反应中失去的电子数目为NA | |
| B. | 17g NH3中所含原子数为4NA | |
| C. | 常温常压下,11.2 LSO3含有的氧原子数为1.5NA | |
| D. | 标准状况下,分子数目为NA氯气所占的体积为22.4L |
分析 A、求出钠的物质的量,然后根据反应后钠元素变为+1价来分析;
B、求出氨气的物质的量,然后根据氨气为4原子分子来分析;
C、常温常压下,三氧化硫为液体;
D、体积V=$\frac{N}{{N}_{A}}Vm$.
解答 解:A、23g钠的物质的量为1mol,而反应后钠元素变为+1价,故1mol钠失去NA个电子,故A正确;
B、17g氨气的物质的量为1mol,而氨气为4原子分子,故1mol氨气中含4mol原子即4NA个,故B正确;
C、常温常压下,三氧化硫为液体,故不能根据气体摩尔体积来计算其物质的量和氧原子个数,故C错误;
D、体积V=$\frac{N}{{N}_{A}}Vm$=$\frac{{N}_{A}}{{N}_{A}/mol}×22.4L\\;/mol$=22.4L,故D正确.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
相关题目
19.NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A. | 含NA个N2和O2的混合气体中质子数不可能是15NA | |
| B. | 1 L 1 mol•L-1的CH3COONa溶液中CH3COOH和CH3COO-的总数为NA | |
| C. | 58g 分子式为C4H10的有机物中,所含有的甲基数一定为2NA | |
| D. | NA个CH4和NA个Cl2光照下充分反应,被取代的氢原子数为2NA |
20.在一定条件下,氯气与碘单质以等物质的量进行反应,可得到一种红棕色液体ICl,ICl有很强的氧化性,ICl跟Zn、H2O反应的化学方程式如下:2ICl+2Zn═ZnCl2+ZnI2 ICl+H2O═HCl+HIO
下列关于ICl性质的叙述正确的是( )
下列关于ICl性质的叙述正确的是( )
| A. | ZnCl2是氧化产物,又是还原产物 | |
| B. | ZnI2是氧化产物,又是还原产物 | |
| C. | ICl跟H2O的反应,ICl是氧化剂,H2O是还原剂 | |
| D. | ICl跟H2O的反应,是自身氧化还原反应 |
1.下列各组离子一定能大量共存的是( )
| A. | 在含有大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- | |
| B. | 25℃,在c(H+)=10-13mol/L的溶液中:NH4+、Al3+、SO42-、NO3- | |
| C. | 能使广泛pH试纸显蓝色的溶液中:Na+、K+、AlO2-、CO32- | |
| D. | 25℃,在pH=0的溶液中:K+、Fe2+、Cl-、NO3- |
18.下列物质的水溶液经加热浓缩,蒸干灼烧仍能得到原物质的是( )
| A. | FeCl3 | B. | Cu(NO3)2 | C. | Na2SO3 | D. | NaAlO2 |
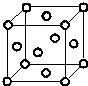 Q、R、X、Y、Z、W为周期表中原子序数依次递增的前四周期元素.
Q、R、X、Y、Z、W为周期表中原子序数依次递增的前四周期元素.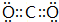 ,分子的空间构型是直线形;Z3+的原子结构示意图为
,分子的空间构型是直线形;Z3+的原子结构示意图为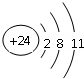 ;X2Q4分子中X原子的杂化方式为sp3杂化.
;X2Q4分子中X原子的杂化方式为sp3杂化.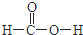 ,m g该物质完全燃烧后通过足量Na2O2固体充分吸收,Na2O2固体增重的质量为$\frac{15m}{23}$g
,m g该物质完全燃烧后通过足量Na2O2固体充分吸收,Na2O2固体增重的质量为$\frac{15m}{23}$g