题目内容
3.研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,同温度下涉及如下反应:a、2NO(g)+Cl2(g)?2ClNO(g)△H1<0 其平衡常数为K1
b、2NO2(g)+NaCl(s)?NaNO3(s)+ClNO(g)△H2<0 其平衡常数为K2
(1)4NO2(g)+2NaCl(s)?2NaNO3(s)+2NO(g)+Cl2(g)△H3的平衡常数K=$\frac{{{K}_{2}}^{2}}{{K}_{1}}$(用K1、K2表示).△H3=2H2-△H1(用△H1、△H2表示).
(2)为研究不同条件对反应a的影响,在恒温条件下,向2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2,10min时反应a达到平衡.测得10min内υ(ClNO)=7.5×10-3mol•L-1•min-1,则平衡后n(Cl2)=0.025mol,NO的转化率α1=75%.其它条件保持不变,反应a在恒压条件下进行,平衡时NO的转化率为α2,α1<α2(填“>”“<”或“=”),平衡常数K1不变(填“增大”“减小”或“不变”).若要使K1减小,可采用的措施是升高温度.
分析 (1)已知:a、NO(g)+Cl2(g)?2ClNO(g),
b、2NO2(g)+NaCl(s)?NaNO3(s)+ClNO(g),
根据盖斯定律,b×2-a可得:4NO2(g)+2NaCl(s)?2NaNO3(s)+2NO(g)+Cl2(g),则该反应平衡常数为b平衡常数平方与a的商;
(2)测得10min内v(ClNO)=7.5×10-3mol•L-1•min-1,则△n(ClNO)=7.5×10-3mol•L-1•min-1×10min×2L=0.15mol,由方程式计算参加反应NO、氯气的物质的量,进而计算平衡时氯气的物质的量、NO的转化率;
正反应为气体物质的量减小的反应,恒温恒容下条件下,到达平衡时压强比起始压强小,其他条件保持不变,反应a在恒压条件下进行,等效为在恒温恒容下的平衡基础上增大压强,平衡正向移动;
平衡常数只受温度影响,温度不变,平衡常数不变,正反应为放热反应,升高温度平衡逆向移动,平衡常数减小.
解答 解:((1)已知:a、NO(g)+Cl2(g)?2ClNO(g),
b、2NO2(g)+NaCl(s)?NaNO3(s)+ClNO(g),
根据盖斯定律,b×2-a可得:4NO2(g)+2NaCl(s)?2NaNO3(s)+2NO(g)+Cl2(g),则该反应平衡常数K=$\frac{{{K}_{2}}^{2}}{{K}_{1}}$,则△H3=2H2-△H1,
故答案为:$\frac{{{K}_{2}}^{2}}{{K}_{1}}$;2H2-△H1;
(2)测得10min内v(ClNO)=7.5×10-3mol•L-1•min-1,则△n(ClNO)=7.5×10-3mol•L-1•min-1×10min×2L=0.15mol,
由方程式可知,参加反应氯气的物质的量为0.15mol×$\frac{1}{2}$=0.075mol,故平衡时氯气的物质的量为0.1mol-0.075mol=0.025mol;
参加反应NO物质的量为0.15mol,则NO的转化率为$\frac{0.15mol}{0.2mol}$×100%=75%;
正反应为气体物质的量减小的反应,恒温恒容下条件下,到达平衡时压强比起始压强小,其他条件保持不变,a在恒压条件下进行,等效为在恒温恒容下的平衡基础上增大压强,平衡正向移动,NO转化率增大,故转化率α1<α2;
平衡常数只受温度影响,温度不变,平衡常数不变,正反应为放热反应,升高温度平衡逆向移动,平衡常数减小,
故答案为:0.025;75%;<;不变;升高温度.
点评 本题考查化学平衡计算与影响因素、化学平衡常数、盖斯定律应用等知识,充分考查学生的分析理解能力,需要学生具备扎实的基础与灵活应用能力,难度中等.

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
| A. | 过程①的提纯是物理过程,过程②通过氧化还原反应可产生2种单质 | |
| B. | 在过程③中将MgCl2•6H2O灼烧即可制得无水MgCl2 | |
| C. | 在过程④、⑥反应中每氧化0.2 mol Br-需消耗0.1mol Cl2 | |
| D. | 除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
| A. | 原溶液中氨水中的c(OH-)与醋酸中的c(H+)相等 | |
| B. | CH3COONH4不发生分解 | |
| C. | 混合溶液中,c(NH3•H2O)=c(CH3COOH) | |
| D. | Kb(NH3•H2O)=3Ka(CH3COOH) |
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(O2)/mol | 0.7 | 0.4 | 0.3 | x | x | x |
(1)用O2表示从0~2s内该反应的平均反应速率为0.4mol•L-1•s-1.
(2)O2的平衡浓度c(O2)=0.5mol•L-1.
(3)求该反应达到平衡时SO2的转化率是90%(用百分数表示).
(4)若将平衡混合气体的5%通入过量的BaCl2溶液,生成沉淀10.5克(计算结果保留一位小数).
| t/min | X/mol | Y/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| 1 | 0.90 | 0.80 | 0.20 |
| 3 | 0.75 | 0.50 | 0.50 |
| 5 | 0.65 | 0.30 | 0.70 |
| 9 | 0.55 | 0.10 | 0.90 |
| 10 | 0.55 | 0.10 | 0.90 |
| 14 | 0.55 | 0.10 | 0.90 |
(2)该反应达到平衡时反应物X的转化率α等于45%;

(3)如果该反应是放热反应.改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线①、②、③(如图2所示),则曲线①、②、③改变的实验条件分别是:
①升高温度;
②使用催化剂;
③增大压强.
 某稀硫酸和稀硝酸的混合溶液200ml,平均分成两份,向其中一份中逐渐加入铜粉,最多能溶解m g.向另一份中逐渐加入铁粉,产生的气体量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体)下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200ml,平均分成两份,向其中一份中逐渐加入铜粉,最多能溶解m g.向另一份中逐渐加入铁粉,产生的气体量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体)下列分析或结果错误的是( )| A. | 第二份溶液中最终溶质为FeSO4 | B. | 原混合酸中NO3-物质的量为0.1mol | ||
| C. | m值为9.6 | D. | H2SO4浓度为2.5mol/L |

 实验室配制500mL 0.2mol•L-1的Na2SO4溶液,实验操作步骤有:
实验室配制500mL 0.2mol•L-1的Na2SO4溶液,实验操作步骤有: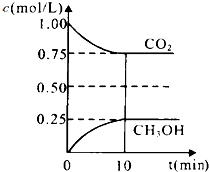 碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一种理想,更是一种值得期待的新的生活方式.在一定温度下的2L固定容积的密闭容器中,通入2molCO2和3mol H2,发生的反应为:CO2(g)+3H2(g)CH3OH(g)+H2O(g),△H=-a kJ•mol-1(a>0),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.
碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一种理想,更是一种值得期待的新的生活方式.在一定温度下的2L固定容积的密闭容器中,通入2molCO2和3mol H2,发生的反应为:CO2(g)+3H2(g)CH3OH(g)+H2O(g),△H=-a kJ•mol-1(a>0),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.