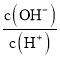题目内容
【题目】弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡。
(1)已知H2A在水中存在以下平衡:H2A=H++HA-,HA-![]() H++A2-。
H++A2-。
①等物质的量浓度的两种溶液:NaHA溶液的pH________(填“大于”“小于”或“等于”)Na2A溶液的pH。NaHA溶液中存在_______个平衡。
②某温度下,若向0.1mol·L-1的NaHA溶液中逐滴滴加0.1mol·L-1 KOH溶液至溶液呈中性。此时该混合溶液中,下列关系中一定正确的是________。
A.c(H+)·c(OH-)=1×10-14
B.c(Na+)+c(K+)=c(HA-)+2c(A2-)
C.c(Na+)<c(K+)
D.c(Na+)+c(K+)=0.1mol·L-1
③已知常温下H2A的钙盐(CaA)的饱和溶液中存在以下平衡:CaA(s)![]() Ca2+(aq)+A2-(aq) ΔH>0。若要使该溶液中Ca2+浓度变小,可采取的措施有________。
Ca2+(aq)+A2-(aq) ΔH>0。若要使该溶液中Ca2+浓度变小,可采取的措施有________。
A.升高温度 B.降低温度 C.加入NH4Cl晶体 D.加入Na2A固体
(2)已知:常温时CH3COOH![]() CH3COO-+H+,Ka=2×10-5则反应CH3COO-+H2O
CH3COO-+H+,Ka=2×10-5则反应CH3COO-+H2O![]() CH3COOH+OH-的平衡常数Kh=________。
CH3COOH+OH-的平衡常数Kh=________。
(3)常温下,若在0.10mol·L-1 CuSO4溶液中加入NaOH稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=________mol·L-1{Ksp[Cu(OH)2]=2.2×10-20}。
【答案】小于 1 B B D 5×10-10 2.2×10-8
【解析】
根据电离程度与水解程度相对大小比较溶液的酸碱性;根据电荷守恒比较溶液中相关离子的浓度大小;根据平衡常数的表达式进行相关计算。
(1)①H2A在水中存在以下平衡:H2A=H++HA,HA![]() H++A2,第一步完全电离,HA离子只存在电离不发生水解,溶液显酸性,Na2A溶液中A2离子水解显碱性,所以NaHA溶液的pH小于Na2A溶液的pH;HA离子只存在电离不发生水解,所以NaHA溶液中存在1个平衡;
H++A2,第一步完全电离,HA离子只存在电离不发生水解,溶液显酸性,Na2A溶液中A2离子水解显碱性,所以NaHA溶液的pH小于Na2A溶液的pH;HA离子只存在电离不发生水解,所以NaHA溶液中存在1个平衡;
②A.水的离子积常数与温度有关,温度越高,水的离子积常数越大,温度未知,所以水的离子积常数未知,故A错误;
B.溶液呈电中性,溶液中阴阳离子所带电荷相等,溶液呈中性,氢离子浓度等于氢氧根离子浓度,所以c(Na+)+c(K+)=c(HA-)+2c(A2-),故B正确;
C.NaHA溶液呈酸性,NaKA溶液呈碱性,向0.1mol·L-1的NaHA溶液中逐滴滴加0.1mol·L-1 KOH溶液至溶液呈中性时,NaHA的物质的量应大于氢氧化钾的物质的量,所以同一混合溶液中c(Na+)>c(K+),故C错误;
D.NaHA溶液呈酸性,向0.1mol·L-1的NaHA溶液中逐滴滴加0.1mol·L-1 KOH溶液至溶液呈中性时,NaHA的体积应大于氢氧化钾的体积,所以c(Na+)+c(K+)>0.1mol·L-1,故D错误;
故答案为:B;
③CaA(s)![]() Ca2+(aq)+A2(aq)△H>0,降温平衡逆向移动,c(Ca2+)减小,加入NH4Cl晶体,铵根离子与A离子水解相互促进,钙离子浓度增大,加入Na2A固体,A离子浓度增大,平衡逆向移动,c(Ca2+)减小,故答案为:BD;
Ca2+(aq)+A2(aq)△H>0,降温平衡逆向移动,c(Ca2+)减小,加入NH4Cl晶体,铵根离子与A离子水解相互促进,钙离子浓度增大,加入Na2A固体,A离子浓度增大,平衡逆向移动,c(Ca2+)减小,故答案为:BD;
(2)根据平衡常数表达式得:![]() ,
,![]() ;
;
(3)根据题给Cu(OH)2的溶度积即可确定pH=8时,c(OH)=10-6mol·L-1,Ksp[Cu(OH)2]=c(Cu2+)×c2(OH)=2.2×10-20,则:c(Cu2+)=![]() 。
。