题目内容
对于Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g)△H<0 的化学反应,下列叙述错误的是( )
A.反应过程中能量关系可用图表示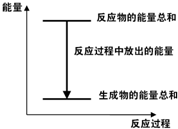 |
| B.若将该反应设计成原电池则锌为负极 |
| C.△H的值与反应方程式的化学计量数有关 |
| D.若将其设计为原电池,当有32.5g锌溶解时,正极放出气体一定为11.2L |
A、该反应是放热反应,说明反应物的能量总和大于生成物的能量总和,故A正确;
B、在电池反应中,金属锌失去电子,而原电池的负极是失电子的极,所以锌为负极,故B正确;
C、△H的值与反应方程式的化学计量数成正比,故C正确;
D、原电池中正极反应是2H++2e-→H2,负极反应是Zn→2e-+Zn2+,当有32.5g(即0.5mol)锌溶解时,转移1mol电子,正极上产生氢气0.5mol,标况下时,体积为才为11.2L,故D错误.
故选D.
B、在电池反应中,金属锌失去电子,而原电池的负极是失电子的极,所以锌为负极,故B正确;
C、△H的值与反应方程式的化学计量数成正比,故C正确;
D、原电池中正极反应是2H++2e-→H2,负极反应是Zn→2e-+Zn2+,当有32.5g(即0.5mol)锌溶解时,转移1mol电子,正极上产生氢气0.5mol,标况下时,体积为才为11.2L,故D错误.
故选D.

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目

