题目内容
11. 对于Zn、Cu和稀H2SO4组成的原电池(如图),下列有关说法正确的是( )
对于Zn、Cu和稀H2SO4组成的原电池(如图),下列有关说法正确的是( )| A. | Cu是负极 | B. | 在外电路中,电流由Zn流向Cu | ||
| C. | Zn电极上发生氧化反应 | D. | Cu极反应:Cu2++2e-═Cu |
分析 锌、铜和稀硫酸组成的原电池中,活泼性较强的锌为原电池的负极,发生:Zn-2e-=Zn2+而被氧化,原电池工作时,电子由负极经外电路流向正极,电解质溶液中,H+流向正极,在Cu棒上得电子被还原为氢气,以此解答该题.
解答 解:A、Zn、Cu、硫酸构成的原电池中,活泼金属锌做负极,金属铜做正极,故A错误;
B、原电池中电流从正极流向负极,即从铜片经导线流向锌片,故B错误;
C、原电池的负极反应是负极金属失电子的氧化反应,故C正确;
D、原电池中金属铜做正极,正极反应是:2H++2e-→H2↑,故D错误;
故选C.
点评 本题考查学生原电池的工作原理,可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目
19.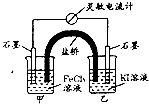 控制合适的条件,将反应2Fe3++2I-?2Fe2++I2设计成如图所示的原电池.下列说法不正确的是( )
控制合适的条件,将反应2Fe3++2I-?2Fe2++I2设计成如图所示的原电池.下列说法不正确的是( )
 控制合适的条件,将反应2Fe3++2I-?2Fe2++I2设计成如图所示的原电池.下列说法不正确的是( )
控制合适的条件,将反应2Fe3++2I-?2Fe2++I2设计成如图所示的原电池.下列说法不正确的是( )| A. | 盐桥中的K+移向FeCl3溶液 | |
| B. | 反应开始时,乙中石墨电极上发生氧化反应 | |
| C. | 电流计读数为零时,反应达到化学平衡状态 | |
| D. | 电流计读数为零后,在甲中溶入FeCl2固体,乙中石墨电级为负极 |
6. 有一种有机化合物,其结构简式如图所示,下列有关它的性质的叙述中,正确的是( )
有一种有机化合物,其结构简式如图所示,下列有关它的性质的叙述中,正确的是( )
 有一种有机化合物,其结构简式如图所示,下列有关它的性质的叙述中,正确的是( )
有一种有机化合物,其结构简式如图所示,下列有关它的性质的叙述中,正确的是( )| A. | 有弱酸性,1mol该有机物与溴水反应,最多能消耗4mol Br2 | |
| B. | 在一定条件下,1mol该物质最多能与6mol NaOH完全反应 | |
| C. | 在Ni催化下,1mol该物质可以和7mol H2发生加成反应 | |
| D. | 它能发生水解反应,水解后只能生成两种产物 |
16.下列物质中,既有离子键,又含有共价键的是( )
| A. | C2H6 | B. | MgCl2 | C. | HNO3 | D. | NaOH |
20.下列关于如图所示原电池装置的叙述中,正确的是( )


| A. | 每当Zn片质量减少65克,Cu片会产生22.4L气体 | |
| B. | 溶液的pH逐渐减小 | |
| C. | 电子从锌片经导线流向铜片 | |
| D. | 氢离子在铜片表面被氧化 |
1.下列有机物不是同一种物质的是( )
| A. |  和 和 | B. | C(CH3)3C(CH3)3和CH3(CH2)3C(CH3)3 | ||
| C. | CH2═CH-CH═CH2和 | D. |  和 和 |





 .稳定性最强的结构式为
.稳定性最强的结构式为 .
.