题目内容
已知A、B、D、E均为中学化学常见单质或化合物。它们之间的关系如下图所示(部分产物略去)。
(1)若A和E为单质,组成A单质的元素是自然界中形成化合物种类最多的元素。
①B属于_________分子(填“极性”或“非极性”),B分子中各原子最外层_________(填“是”或“否”)都满足8电子结构;
②向50 mL 4 mol·L-1的NaOH溶液中通入
③
(2)若A为第三周期中的元素所形成的氯化物。
①写出A溶液B的离子方程式_________________________;
②写出A和B的溶液反应的离子方程式________________________。
(3)若A为常见的金属,在E的冷、浓溶液中,A有钝化现象。已知:X为含有非极性键的离子化合物,且1 mol X含有38 mol电子,向D溶液中加入与D等物质的量的X固体,恰好完全反应,写出该反应的离子方程式________________________。
(1)①非极性 是 ②Na2CO3:NaOH=1:2 ③C(s)+O2(g)![]() CO2(g);ΔH=-393.6 kJ·mol-1
CO2(g);ΔH=-393.6 kJ·mol-1
(2)①Al3++4OH-![]()
![]() +2H2O②Al3++3
+2H2O②Al3++3![]() +6H2O
+6H2O![]() 4Al(OH)3↓
4Al(OH)3↓
(3)4Fe2++4Na2O2+6H2O![]() 4Fe(OH)3+O2↑+8Na+
4Fe(OH)3+O2↑+8Na+
解析:(1)①组成A单质的元素为碳,则E为O2,B为CO2,属于非极性分子,CO2分子中各原子最外层都满足8电子结构;
②2NaOH + CO2 ![]() Na2CO3+H2O
Na2CO3+H2O
0.2 mol 0.05 mol
生成Na2CO3 0.05 mol,剩余NaOH 0.1 mol.
(2)若A为第三周期元素形成的氯化物,则A只能是AlCl3,E为NaOH,可据此写出相关的离子方程式.
(3)A为常见金属,并且与E反应时能显示不同价态,故A为Fe.X为Na2O2.根据氧化还原方程式的书写原则,可写出Na2O2与Fe2+反应的离子方程式
4Fe2++4Na2O2+6H2O![]() 4Fe(OH)3+O2↑+8Na+.
4Fe(OH)3+O2↑+8Na+.

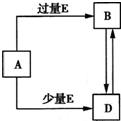 已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去).下列说法错误的是( )
已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去).下列说法错误的是( ) 已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去).
已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去).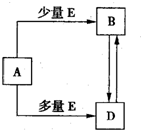 已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去).
已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去).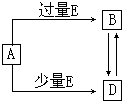 已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去).
已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去).