题目内容
12.对于反应Zn+H2SO4═ZnSO4+H2↑,下列措施能增大氢气生成速率的是( )| A. | 使用18.4 mol•L-1的硫酸 | B. | 升高溶液的温度 | ||
| C. | 向溶液中加入少量硝酸 | D. | 把锌粉换成锌块(片) |
分析 根据方程式知,适当增大稀硫酸浓度、增大反应物接触面积、升高温度等方法都能加快反应速率,据此分析解答.
解答 解:A.浓硫酸和锌反应生成二氧化硫而不是氢气,故A错误;
B.升高温度,增大活化分子百分数,所以反应速率增大,故B正确;
C.向溶液中加入少量硝酸,硝酸和锌反应生成氮氧化物而不是氢气,故C错误;
D.将锌粉换成锌块,减少反应物接触面积,则反应速率降低,故D错误;
故选B.
点评 本题考查化学反应速率影响因素,为高频考点,温度、浓度、压强、催化剂等影响化学反应速率,注意外界条件的适用范围,易错选项是AC.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2.37Cl是氯的一种同位素,下列说法正确的是( )
| A. | $\frac{1}{40}$mol的1H37Cl分子所含中子数约为3.01×1023 | |
| B. | 37Cl原子所含质子数为20 | |
| C. | 37Cl2气体的摩尔质量为74 | |
| D. | 3.7g37Cl2气体的体积约为22.4L |
3.已知乙烯能被酸性高锰酸钾溶液氧化成CO2.既可以用来鉴别乙烷和乙烯,又可以用来除去乙烷中混有的乙烯的方法是( )
| A. | 通入酸性高锰酸钾溶液中 | B. | 通入足量溴水中 | ||
| C. | 通入水中 | D. | 在空气中燃烧 |
7.实验中需2mol/L的NaCl溶液950mL,配制时应选用的容量瓶的规格和称取NaCl的质量分别( )
| A. | 1000mL,117g | B. | 950mL,111.2 g | C. | 任意规格,117g | D. | 500mL,111.2g |
17.某有机物的结构图,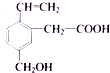 下列说法不正确的是( )
下列说法不正确的是( )
 下列说法不正确的是( )
下列说法不正确的是( )| A. | 能使Br2的四氯化碳溶液褪色 | B. | 能发生酯化反应 | ||
| C. | 该有机物的分子式C11H13O3 | D. | 能与金属钠发生反应 |
1.下列可用于区别苯、甲苯、苯酚、四氯化碳四种无色液体的一组试剂为( )
| A. | 氯化铁溶液、溴水 | B. | NaOH溶液、溴水 | ||
| C. | NaHCO3溶液、溴水 | D. | 高锰酸钾溶液、溴水 |
2.某10% NaOH溶液,加热蒸发掉100g水后得到80mL 20% 的溶液,则该20% NaOH溶液的物质的量浓度为
( )
( )
| A. | 5.25 mol/L | B. | 12.5 mol/L | C. | 7.5 mol/L | D. | 6.25 mol/L |

 ,该反应类型为取代反应.
,该反应类型为取代反应. .
. .
. .
.