题目内容
为了提高生活用水的卫生标准,自来水厂最好选用下列哪种物质来作净化剂( )
| A、氯化铜 | B、明矾 |
| C、硫酸铜 | D、氯化铁 |
考点:盐类水解的应用
专题:盐类的水解专题
分析:胶体具有吸附性而作净水剂,作净水剂的物质不能对人体健康产生危害,据此分析解答.
解答:
解:A.铜元素属于重金属,过量易导致人产生重金属中毒现象,故A错误;
B.铝水解生成氢氧化铝胶体,胶体能吸附水中的悬浮物而净水,但铝过量易产生老年痴呆症,故B错误;
C.铜元素属于重金属,过量易导致人产生重金属中毒现象,故C错误;
D.铁可以在水中水解生成胶体,可以起到净化作用,铁离子对人类有益处的,故D正确;
故选D.
B.铝水解生成氢氧化铝胶体,胶体能吸附水中的悬浮物而净水,但铝过量易产生老年痴呆症,故B错误;
C.铜元素属于重金属,过量易导致人产生重金属中毒现象,故C错误;
D.铁可以在水中水解生成胶体,可以起到净化作用,铁离子对人类有益处的,故D正确;
故选D.
点评:本题考查了净水剂的选取,知道常见金属元素的性质,根据物质的性质来分析解答,题目难度不大.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
下列关于化学反应速率、化学反应限度的说法中错误的是( )
| A、其他条件不变时,升高温度,化学反应速率加快 |
| B、其他条件不变时,增大反应物的浓度,化学反应速率加快 |
| C、化学反应达到一定限度即“平衡状态”时,正反应的速率与逆反应的速率相等 |
| D、化学反应达到一定限度即“平衡状态”时,反应物的浓度与生成物的浓度相等 |
下列离子方程式正确的是( )
| A、水玻璃中通入二氧化碳:Na2SiO3+CO2+H2O=H2SiO3+CO32-+2Na+ |
| B、向氯化亚铁溶液中通入少量氯气:Fe2++Cl2=Fe3++2Cl- |
| C、硫酸厂的废气SO2用强碱溶液吸收:SO2+2OH-═SO42-+H2O |
| D、SiO2溶于NaOH溶液:SiO2+2OH-=SiO32-+H2O |
化学反应的特征是( )
| A、发光 | B、能量发生变化 |
| C、状态发生变化 | D、发热 |
下列有机物一氯取代物的同分异构体数目相等的是( )
① ②
② ③
③ ④
④
①
 ②
② ③
③ ④
④
| A、①和② | B、②和③ |
| C、③和④ | D、①和③ |
现有等体积的Ba(OH)2、NaOH和NH3?H2O三种溶液,将它们分别与V1 L、V2 L、V3 L等浓度的盐酸混合,下列说法中正确的是( )
| A、若混合前三溶液物质的量浓度相等,混合后溶液呈中性,则V1>V2=V3 |
| B、若混合前三溶液pH相等,酸碱恰好完全反应,则V1=V2<V3 |
| C、若混合前三溶液物质的量浓度相等,酸碱恰好完全反应,则V1=V2=V3 |
| D、若混合前三溶液pH相等,将它们同等倍数稀释后,则NaOH溶液pH最大 |
下列说法不正确的是( )

A、在25℃时,将c mol?L-1的醋酸溶液与0.02mol?L-1 NaOH溶液等体积混合后溶液刚好呈中性,用含c的代数式表示CH3COOH的电离常数Ka=
| ||
| B、0.1mol?L-1醋酸溶液中:c(H+)2=c(H+)?c(CH3COO-)+KW | ||
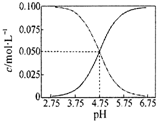
| C、常温下醋酸和醋酸钠混合溶液中c(CH3COOH)、c(CH3COO-)与pH值的关系如右图所示,当pH=4.5溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) | ||
| D、等体积等物质的量浓度的CH3COONa(aq)与NaCl(aq)中离子总数大小:N前>N后 |