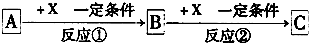题目内容
3.下列表述正确的是( )①某物质经科学测定只含有一种元素,不可以断定该物质一定是一种纯净物;
②过量铁粉在氯气中燃烧生成FeCl2
③浓硝酸在光照条件下变黄,说明浓硝酸不稳定,生成的有色产物能溶于浓硝酸;
④医疗上用的“钡餐”其成分是碳酸钡,漂白粉的成分为次氯酸钙;
⑤高压钠灯发出的黄光射程远,透雾能力强,故可做航标灯
⑥能与酸反应的氧化物,一定是碱性氧化物.
| A. | ①②③ | B. | ①③⑤ | C. | ②④⑥ | D. | ②③⑤ |
分析 ①一种元素组成的物质不一定是纯净物,同素异形体组成的混合物含一种元素;
②氯气具有强氧化性,和变价金属铁反应生成高价化合物;
③硝酸不稳定,在光照条件下易分解生成二氧化氮,二氧化氮溶于硝酸而使溶液呈黄色;
④漂白粉的成分为次氯酸钙、氯化钙,有效成分是次氯酸钙;
⑤钠的焰色反应为黄色;
⑥能与酸反应只生成盐和水的氧化物属于碱性氧化物.
解答 ①一种元素组成的物质不一定是纯净物,同素异形体组成的混合物含一种元素如O2、O3的混合物;故①正确;
②氯气具有强氧化性,和变价金属铁反应生成高价化合物,固体状态铁过量不与氯化铁反应,铁在溶液中和氯化铁反应生成氯化亚铁,故②错误;
③硝酸不稳定,在光照条件下易分解生成二氧化氮,二氧化氮溶于硝酸而使溶液呈黄色,所以浓硝酸溶液呈黄色,故③正确;
④医疗上用的“钡餐”其成分是硫酸钡,漂白粉的成分为次氯酸钙、氯化钙,有效成分是次氯酸钙,故④错误;
⑤钠的焰色反应为黄色,由于射程远,透雾能力强,故可做航标灯,故⑤正确.
⑥能与酸反应的氧化物不一定是碱性氧化物,例如过氧化钠、氧化铝都能与酸反应,但是不属于碱性氧化物,故⑥错误;
故选B.
点评 本题考查较为综合,涉及物质分类、物质的性质、物质应用等,侧重于基础知识的考查,注意相关基础知识的积累,题目难度不大.

练习册系列答案
相关题目
14.铝土矿的主要成分为氧化铝,还有少量的氧化铁和二氧化硅杂质.工业上经过下列工艺可以冶炼金属铝:
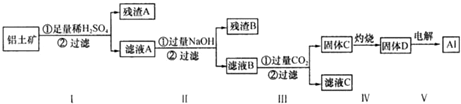
下列说法中正确的是( )

下列说法中正确的是( )
| A. | 滤液A 可用于净水,其净水原理为Al3++3H2O═Al(OH)3+3H+ | |
| B. | 固体C→固体D 的操作过程中主要仪器是酒精灯、蒸发皿、玻璃棒 | |
| C. | 滤液C 中存在以下关系:c(Na+)=c(SO42-)+2 c(CO32-)+c(HCO3-)+c(OH-)-c(H+) | |
| D. | 若在100 mL 滤液B 中加入1 mol•L-1HCl 200 mL,沉淀达到最大且质量为11.7 g,则滤液B 中c(Na+)大小2 mol•L |
18.下列反应的离子方程式正确的是( )
| A. | 明矾可以净水:Al3++3H2O=Al(OH)3(胶体)↓+3H+ | |
| B. | 少量小苏打溶液滴入Ba(OH)2溶液中:HCO-3+Ba2++OH-=BaCO3↓+H2O | |
| C. | 硫氢化钠发生水解:HS-+H2O?H3O++S2- | |
| D. | 氧化亚铁加入稀硝酸:FeO+2H+=Fe2++H2O |
8.为研究某铁钉与浓硫酸反应生成气体Y的成分,某学习小组做出假设,认为所得气体中除含有SO2外,还可能含有H2和Q气体,并设计了下列实验装置(图中夹持仪器省略)探究气体的成分,为确认Q的存在,需在装置中添加M于( )


| A. | A-B之前 | B. | B-C间 | C. | C-D间 | D. | D-E间 |
15.在某学生的化学实验报告中有如下记录其中实验数据合理的( )
| A. | 用托盘天平称取11.7 g CuO粉末 | |
| B. | 用100 mL量筒量取5.26 mL稀硫酸溶液 | |
| C. | 温度计上显示的室温读数为25.68℃ | |
| D. | 用广泛pH试纸测得溶液的pH为3.5 |
12.下列说法不正确的是( )
| A. | 碘易升华,应该密封保存 | |
| B. | 液溴应保存在磨口玻璃塞深棕色细口试剂瓶中,并加少量水进行水封 | |
| C. | 酒精与水互溶,所以不能用酒精把碘从碘水中萃取出来 | |
| D. | 用加热的方法可以将NH4Cl与碘的混合物分离 |
13.设NA为阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 1mol丙烷分子中,含有的非极性共价键数目为NA | |
| B. | 标准状况下,1.8gH2O分子中所含有的电子数为NA | |
| C. | 25℃时,pH=13的 Ba(OH)2溶液中含有的OH-数目为0.1 NA | |
| D. | 2.24L 氯气与过量的氢氧化钠溶液完全反应转移的电子数为0.1NA |
 金属腐蚀造成很大的经济损失,甚至超过自然灾害,其中钢铁锈蚀最为严重,寻求防止钢铁腐蚀的方法意义重大.
金属腐蚀造成很大的经济损失,甚至超过自然灾害,其中钢铁锈蚀最为严重,寻求防止钢铁腐蚀的方法意义重大.