题目内容
用下列装置进行以下实验:加热白色固体A(A灼烧时火焰为黄色)生成白色固体B,并放出气体C和D,气体D与淡黄色固体E 反应,生成固体B 和气体F.
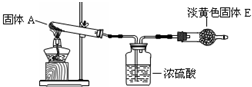
试回答下列问题:
(1)写出下列物质的化学式:
A
(2)写出下列反应的离子方程式:
①向B的稀溶液中通入D:
②向A的溶液中滴加氢氧化钠溶液:

试回答下列问题:
(1)写出下列物质的化学式:
A
NaHCO3
NaHCO3
DCO2
CO2
ENa2O2
Na2O2
FO2
O2
.(2)写出下列反应的离子方程式:
①向B的稀溶液中通入D:
CO32-+CO2+H2O=2HCO3-
CO32-+CO2+H2O=2HCO3-
;②向A的溶液中滴加氢氧化钠溶液:
HCO3-+OH-=CO32-+H2O
HCO3-+OH-=CO32-+H2O
.分析:加热白色固体A(A灼烧时火焰为黄色)生成白色固体B,并放出气体C和D,则A、B含有Na元素,气体D与淡黄色固体E反应,生成固体B和气体F,应是Na2O2与CO2反应生成Na2CO3与O2,可推知D为CO2,E为Na2O2,B为Na2CO3,F为O2,故A为NaHCO3,C为水蒸气,据此解答.
解答:解:加热白色固体A(A灼烧时火焰为黄色)生成白色固体B,并放出气体C和D,则A、B含有Na元素,气体D与淡黄色固体E反应,生成固体B和气体F,应是Na2O2与CO2反应生成Na2CO3与O2,可推知D为CO2,E为Na2O2,B为Na2CO3,F为O2,故A为NaHCO3,C为水蒸气,
(1)由上述分析可知,A为NaHCO3,D为CO2,E为Na2O2,F为O2,
故答案为:NaHCO3;CO2;Na2O2;O2;
(2)①向Na2CO3的稀溶液中通入CO2,反应生成碳酸氢钠,反应离子方程式为:CO32-+CO2+H2O=2HCO3-,
故答案为:CO32-+CO2+H2O=2HCO3-;
②向NaHCO3的溶液中滴加氢氧化钠溶液,反应生成碳酸钠与水,反应离子方程式为:HCO3-+OH-=CO32-+H2O,
故答案为:HCO3-+OH-=CO32-+H2O.
(1)由上述分析可知,A为NaHCO3,D为CO2,E为Na2O2,F为O2,
故答案为:NaHCO3;CO2;Na2O2;O2;
(2)①向Na2CO3的稀溶液中通入CO2,反应生成碳酸氢钠,反应离子方程式为:CO32-+CO2+H2O=2HCO3-,
故答案为:CO32-+CO2+H2O=2HCO3-;
②向NaHCO3的溶液中滴加氢氧化钠溶液,反应生成碳酸钠与水,反应离子方程式为:HCO3-+OH-=CO32-+H2O,
故答案为:HCO3-+OH-=CO32-+H2O.
点评:本题考查无机物推断,涉及钠元素化合物性质转化关系、常用化学用语等,难度不大,掌握过氧化钠的特殊性质是关键,注意基础知识的理解掌握.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
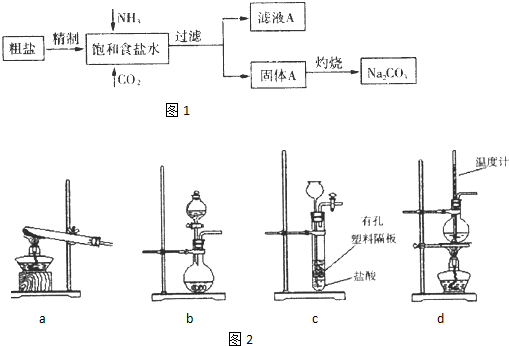

 NaHCO3↓+NH4Cl,请回答以下问题:
NaHCO3↓+NH4Cl,请回答以下问题: