题目内容
在0.5L某浓度的NaOH溶液中含有0.5mol Na+,下列对该溶液的说法中不正确的是( )
| A、该溶液物质的量浓度为1mol?L-1 |
| B、该溶液中含有40g NaOH |
| C、配制100mL该溶液需用4.0g NaOH |
| D、量取100mL该溶液倒入烧杯中,烧杯中Na+的物质的量为0.1mol |
考点:物质的量浓度的相关计算
专题:物质的量浓度和溶解度专题
分析:A、溶液的浓度c=c(Na+)=
;
B、氢氧化钠的物质的量等于钠离子的物质的量,带入m=n?M计算;
C、根据n=c?V计算物质的量,带入m=n?M计算质量;
D、钠离子的物质的量与溶液的体积呈正比.
| 0.5mol |
| 0.5L |
B、氢氧化钠的物质的量等于钠离子的物质的量,带入m=n?M计算;
C、根据n=c?V计算物质的量,带入m=n?M计算质量;
D、钠离子的物质的量与溶液的体积呈正比.
解答:
解:A、溶液的浓度c=c(Na+)=
=1mol/L,故A正确;
B、氢氧化钠的物质的量等于钠离子的物质的量为0.5mol,氢氧化钠的质量为0.5mol×40g/mol=20g,故B错误;
C、100ml溶液中含有氢氧化钠的物质的量n=c?V=1mol/L×0.1L=0.1mol,需要氢氧化钠的质量m=0.1mol×40g/mol=4.0g,故C正确;
D、500ml溶液中含有0.5mol Na+,则100ml溶液中含有0.1molNa+,故D正确;
故选B.
| 0.5mol |
| 0.5L |
B、氢氧化钠的物质的量等于钠离子的物质的量为0.5mol,氢氧化钠的质量为0.5mol×40g/mol=20g,故B错误;
C、100ml溶液中含有氢氧化钠的物质的量n=c?V=1mol/L×0.1L=0.1mol,需要氢氧化钠的质量m=0.1mol×40g/mol=4.0g,故C正确;
D、500ml溶液中含有0.5mol Na+,则100ml溶液中含有0.1molNa+,故D正确;
故选B.
点评:本题考查离子物质的量浓度的有关计算,难度不大,注意电解质离子浓度与电解质浓度关系.

练习册系列答案
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
晨的树林,可以观测到一束束的阳光透过树叶,射入林间,这是种现象源自胶体的( )
| A、丁达尔效应 | B、聚沉 |
| C、电泳 | D、折射 |
下列说法正确的是( )
| A、强电解质溶液一定比弱电解质溶液的导电性强 |
| B、强电解质的水溶液中不存在电解质分子 |
| C、强电解质都是离子化合物,弱电解质都是共价化合物 |
| D、不同的弱电解质只要物质的量浓度相同,电离程度也就相同 |
标准状况下,两个容积相等的贮气瓶,一个装有O2,另一个装有O3,两瓶气体具有相同的( )
| A、质量 | B、原子总数 |
| C、密度 | D、分子数 |
 已知常温时CH3COOH的电离平衡常数为K.该温度下向20mL 0.1mol?L-1CH3COOH溶液中逐滴加入0.1mol?L-1NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中错误的是( )
已知常温时CH3COOH的电离平衡常数为K.该温度下向20mL 0.1mol?L-1CH3COOH溶液中逐滴加入0.1mol?L-1NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中错误的是( )| A、b点表示的溶液中c(CH3COO-)>c(Na+) | ||
| B、c点表示CH3COOH和NaOH恰好反应完全 | ||
| C、a、b点间一定存在c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | ||
D、b、d点表示的溶液中
|
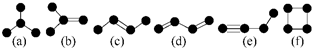 如图所示是4个碳原子相互结合的方式.小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢结合.则下列说法中正确的是( )
如图所示是4个碳原子相互结合的方式.小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢结合.则下列说法中正确的是( )| A、一个有机物a分子中含有8个氢原子 |
| B、有机物b、c、f互为同分异构体 |
| C、有机物d、e的1H核磁共振谱中,特征峰的数目相同 |
| D、有机物b、c、e中4个碳原子可处于同一平面 |
对配合物[Cu(NH3)4]SO4的叙述,错误的是( )
| A、Cu2+和NH3之间以配位键结合 | ||
B、[Cu(NH3)4]2+和SO
| ||
| C、Cu2+和NH3之间以离子键结合 | ||
D、[Cu(NH3)4]SO4在水中全部电离成[Cu(NH3)4]2+和SO
|
物质的量浓度相同的下列各溶液①NaHSO4 ②NaHCO3 ③Na2CO3 ④Na2SO4,由水电离出的氢氧根浓度由大到小的顺序( )
| A、④③②① | B、①②③④ |
| C、③②④① | D、③④②① |
下列关于盐类水解反应的应用说法正确的是( )
| A、可以把FeCl3固体直接溶于水制FeCl3溶液 |
| B、热的纯碱溶液去油污效果好 |
| C、加热AlCl3溶液可得到AlCl3固体 |
| D、Mg粉投入到饱和NH4Cl溶液中无明显现象 |